
Artikel überprüft von: Dr. Sturz Ciprian, Dr. Tîlvescu Cătălin und Dr. Alina Vasile
Alles, was Sie über Peptide wissen müssen: von der Wissenschaft der Regeneration bis hin zu Forschungsprotokollen
- Was sind Peptide?
- Warum interessieren Peptide die kardiovaskuläre Medizin
- Injizierbare Peptide: die am meisten erforschten und am häufigsten diskutierten
- Orale Peptide: eine biologische Herausforderung und ein reales Versprechen
- Topische Peptide: die zugänglichsten und mit den solidesten Nachweisen beim Menschen
- Matrixyl (Palmitoyl Pentapeptid-4), das Referenz-Anti-Aging-Peptid
- Argireline (Acetyl Hexapeptid-3) — die kosmetische Alternative zu Botox
- Orale hydrolysierte Kollagenpeptide — was die interne Supplementierung bringt
- GHK-Cu — das Kupferpeptid mit drei Jahrzehnten Forschung
- Topisches Thymosin Beta-4 — das Peptid für die Heilung schwieriger Wunden
- Forschungspeptide: vielversprechend im Labor, derzeit nicht für die Anwendung beim Menschen zugelassen
- Wie die hyperbare Therapie die natürliche Peptidproduktion im Körper stimuliert
- Warum die hyperbare Therapie heute die sichere Wahl ist
- Die Zukunft der Peptide: wohin sich die Forschung entwickelt
Wenn Sie kürzlich von Peptiden gehört haben, in einer Arztpraxis, im Internet oder in einem Podcast über Langlebigkeit, und sich gefragt haben, was sie sind, ob sie wirklich wirken und ob sie sicher sind, sind Sie hier genau richtig. Peptide sind zu einem der meistdiskutierten Themen der modernen Medizin geworden, und das nicht ohne Grund. Forscher entdecken, dass diese winzigen Moleküle, die unser Körper auf natürliche Weise produziert, ein bemerkenswertes regeneratives Potenzial haben, von der Heilung von Gewebe und der Herzgesundheit bis hin zur Erholung nach einem Schlaganfall.
Doch bevor man sich von Begeisterung mitreißen lässt, ist es wichtig zu verstehen, was wir genau wissen, was wir noch nicht wissen und wo die Grenze zwischen Versprechen und klinischer Realität liegt. Dieser Artikel erklärt alles: die Arten von Peptiden, was medizinische Studien sagen, wie sie eingesetzt werden und, gegen Ende, warum die medizinische hyperbare Therapie derzeit eine der sichersten und am besten dokumentierten Optionen für die Gesundheit von Herz und Gehirn bleibt.
Was sind Peptide?
Stellen Sie sich die Proteine in Ihrem Körper wie lange Ketten aus Gliedern vor. Jedes Glied ist eine Aminosäure. Ein Peptid ist im Grunde ein kurzes Fragment einer solchen Kette, also einige miteinander verbundene Glieder, normalerweise zwischen 2 und 50 Aminosäuren. Wird die Kette länger als 50, spricht man bereits von einem Protein.
Was Peptide besonders macht, ist nicht ihre geringe Größe, sondern die Präzision, mit der sie wirken. Jedes Peptid passt wie ein Schlüssel in ein spezifisches Schloss, einen Rezeptor auf der Oberfläche der Zellen, und übermittelt eine präzise Botschaft: „baue Kollagen“, „bilde neue Blutgefäße“, „reduziere Entzündungen“, „repariere geschädigtes Gewebe“. Der menschliche Körper produziert auf natürliche Weise Hunderte solcher Botenstoffe. Insulin ist ein Peptid. Oxytocin ist ein Peptid. Wachstumshormon wirkt über Peptide. Die Idee hinter der Peptidtherapie ist einfach: Wenn diese Moleküle bereits im Körper existieren und Gutes bewirken, können wir sie dann therapeutisch nutzen oder stimulieren?
Die Antwort der Forschung lautet: ja, aber mit vielen Nuancen.
Warum interessieren Peptide die kardiovaskuläre Medizin
Das kardiovaskuläre System ist wahrscheinlich der Bereich, in dem Peptide das größte regenerative Potenzial gezeigt haben. Der Grund ist einfach: Das Herz ist ein Organ mit einer extrem begrenzten Fähigkeit zur Selbstregeneration. Während Niere oder Leber bis zu einem gewissen Grad kompensieren können, kann das Herz verlorene Muskelzellen nach einem Infarkt nicht effizient ersetzen. Genau hier kommen Peptide ins Spiel, als potenzielle „Architekten“ eines Regenerationsprozesses, den der Körper allein nicht vollständig durchführen kann.
Und der epidemiologische Kontext macht diese Diskussion dringend. Laut Nationalem Institut für öffentliche Gesundheit sind Herz-Kreislauf-Erkrankungen für fast 56 % aller Todesfälle in Rumänien verantwortlich. Laut Daten des Gesundheitsministeriums ist die kardiovaskuläre Sterblichkeitsrate in Rumänien 2,5-mal höher als der Durchschnitt der Europäischen Union.
Und Bluthochdruck, einer der wichtigsten Risikofaktoren, betrifft mehr als 45 % der Erwachsenen in Rumänien, laut der Rumänischen Gesellschaft für Hypertonie. Diese Zahlen sind keine abstrakten Statistiken. Sie beschreiben eine Krise der öffentlichen Gesundheit, in der jede neue therapeutische Option ernst genommen werden sollte.
Injizierbare Peptide: die am meisten erforschten und am häufigsten diskutierten
Injizierbare Peptide sind die Kategorie mit dem größten Forschungsvolumen und zugleich mit dem größten Interesse der informierten Öffentlichkeit. Der Grund, warum Injektionen gegenüber dem Schlucken einer Tablette bevorzugt werden, ist einfach: Unser Magen zerlegt Peptide wie jedes andere Protein. Verdauungsenzyme zerlegen sie in Stücke, bevor das aktive Molekül den Blutkreislauf erreicht. Die subkutane (unter die Haut) oder intramuskuläre Injektion umgeht dieses Problem und ermöglicht es dem Peptid, intakt in den Kreislauf zu gelangen.
BPC-157 — das Peptid aus dem Magensaft
Wenn man ein einzelnes Peptid wählen müsste, das in der medizinischen Forschung des letzten Jahrzehnts das größte Interesse geweckt hat, wäre es mit großer Wahrscheinlichkeit BPC-157. Nicht wegen seines besonders spektakulären Namens, die Abkürzung steht für „Body Protective Compound 157“, sondern wegen der ungewöhnlich breiten Wirkungspalette, die in Studien für ein so kleines Molekül dokumentiert wurde.
Sein Ursprung ist auf den ersten Blick überraschend: Es handelt sich um eine Sequenz von 15 Aminosäuren, die aus einem Protein stammt, das natürlicherweise im menschlichen Magensaft vorkommt. Unser Magen produziert es ständig, und Forscher haben im Laufe der Zeit beobachtet, dass der Verdauungstrakt eine bemerkenswerte Fähigkeit besitzt, sich schnell nach Verletzungen zu regenerieren. Die naheliegende Frage war: Hat BPC-157 etwas mit dieser Fähigkeit zu tun? Und wenn ja, kann es auch in anderen Geweben eingesetzt werden?
Die bisherigen Forschungsergebnisse liefern, mit der gebotenen Vorsicht, eine bejahende Antwort. Eine 2025 veröffentlichte systematische Analyse von Forschern der Case Western Reserve University im HSS Journal, "Emerging Use of BPC-157 in Orthopaedic Sports Medicine", wertete 544 Artikel aus und umfasste 36 Studien. Das Fazit? BPC-157 stimuliert die Produktion von VEGF (dem Wachstumsfaktor für Blutgefäße), aktiviert zelluläre Vermehrungswege und reduziert entzündliche Zytokine, also Moleküle, die chronische Entzündungen aufrechterhalten. Einfach ausgedrückt: Dieses Peptid scheint den Zellen zu sagen: bildet neue Blutgefäße, vermehrt euch und stoppt die Entzündung. Alle drei Prozesse sind entscheidend nach einem Herzinfarkt oder jeder anderen Gewebeschädigung.
Eine weitere 2025 in PMC veröffentlichte Studie, "Regeneration or Risk? A Narrative Review of BPC-157", bestätigt, dass BPC-157 die Produktion von Stickstoffmonoxid stimuliert, einem Molekül, das Blutgefäße nutzen, um sich zu erweitern und einen besseren Blutfluss zu ermöglichen. Wenn Gefäße zu wenig Stickstoffmonoxid produzieren (wie bei Atherosklerose, Diabetes oder Bluthochdruck), fließt das Blut schlechter, der Druck steigt und das Risiko eines Herzinfarkts nimmt zu. BPC-157 scheint diesen natürlichen Mechanismus reaktivieren zu können.
Eine Studie aus dem Jahr 2025, "Protective Effects of BPC-157 on Liver, Kidney, and Lung Following Lower Extremity Ischemia-Reperfusion", zeigte, dass das Peptid Leber, Nieren und Lunge vor Schäden durch Blutmangel und dessen plötzliche Wiederherstellung schützte, ein Mechanismus, der als „Reperfusionsverletzung“ bekannt ist und im Zusammenhang mit Herzinfarkten relevant ist.
All das klingt vielversprechend. Und das ist es auch. Doch es gibt eine wesentliche Nuance, die jeder ehrliche Artikel klar benennen muss: BPC-157 ist weder in der Europäischen Union noch von der FDA als Medikament zugelassen für irgendeine Anwendung beim Menschen. Alle genannten Studien wurden an Tieren durchgeführt. BPC-157 wird rechtlich ausschließlich als Forschungsstoff vermarktet, also für den Laboreinsatz, nicht für den menschlichen Konsum. Das langfristige Sicherheitsprofil beim Menschen ist unbekannt. Das mindert nicht den Wert der Forschung, bedeutet aber, dass eine Anwendung ohne sorgfältige medizinische Überwachung und ohne klares Verständnis der Grenzen der aktuellen Evidenz nicht verantwortbar ist.
TB-500 und Thymosin Beta-4, das Alarmsignal der Blutgefäße
Im Körper existiert ein bemerkenswertes biologisches Notfallsystem: Wenn ein Gewebe verletzt wird, senden die Zellen rund um die Wunde chemische Signale aus, die Reparaturzellen aus anderen Teilen des Körpers „herbeirufen“, einschließlich aus dem Knochenmark, wo Stammzellen gespeichert sind. Thymosin Beta-4 ist eines der Moleküle, die diese Mobilisierung koordinieren. Es wird natürlich vom Thymus produziert, einer Immun-Drüse hinter dem Brustbein, etwa so groß wie eine Feige, und spielt eine zentrale Rolle bei der Mobilisierung endothelialer Vorläuferzellen, also jener „prä-vaskulären“ Zellen, die zur Reparatur geschädigter Blutgefäße beitragen können. TB-500 ist eine synthetische Variante seines aktiven Fragments, entwickelt, um diese Mobilisierungs- und Reparaturfunktion nachzuahmen.
Eine 2024 in der Zeitschrift Angiogenesis veröffentlichte Studie, "Restoration of Blood Vessel Regeneration in the Era of Advanced Therapies", zeigt, dass Thymosin Beta-4 die Migration endothelialer Zellen in geschädigte Bereiche stimuliert, Entzündungen der Gefäßwand reduziert und die Bildung neuer Kapillaren fördert. Kapillaren sind die kleinsten Blutgefäße im Körper, ein mit bloßem Auge unsichtbares Netzwerk, aber essenziell, da sie die Versorgung einzelner Zellen sicherstellen. Wenn ein Herzinfarkt oder ein Schlaganfall dieses feine Netzwerk zerstört, erhalten Gewebe keinen Sauerstoff und keine Glukose mehr, selbst wenn die großen Arterien wieder durchblutet werden. Thymosin Beta-4 könnte helfen, dieses Netzwerk wieder aufzubauen, ein Effekt, den keine aktuelle Therapie direkt adressiert.
Eine in PLOS ONE veröffentlichte Studie zeigte, dass TB-4 in experimentellen Modellen die Re-Epithelisierung von Wunden um bis zu 61 % im Vergleich zur Kontrollgruppe erhöhte, mit einer signifikanten Zunahme der Kollagenablagerung und lokalen Angiogenese. Die Migration von Zellen, die die Haut bedecken und schützen, war 2- bis 3-mal höher als in der unbehandelten Gruppe, bei extrem niedrigen Dosen im Picogrammbereich. Dies deutet darauf hin, dass TB-4 als Signal mit geringer Intensität wirkt, aber eine überproportional starke biologische Wirkung entfaltet.
Wie BPC-157 wird auch TB-500 ausschließlich zu Forschungszwecken vermarktet und ist nicht für die therapeutische Anwendung beim Menschen in der EU oder den USA zugelassen
CJC-1295 und Ipamorelin, die Peptide, die das Wachstumshormon stimulieren
Bisher haben wir über Peptide gesprochen, die direkt auf Gewebe wirken, also auf Blutgefäße, Muskeln und Haut. Es gibt jedoch eine weitere Kategorie von Peptiden mit einem völlig anderen Mechanismus: Statt direkt zu reparieren, aktivieren sie die Hypophyse. Dies ist eine kleine Drüse an der Basis des Gehirns, etwa so groß wie eine Erbse, die die Produktion mehrerer essenzieller Hormone steuert, einschließlich des Wachstumshormons (GH). CJC-1295 und Ipamorelin sind zwei Peptide, die die Hypophyse dazu stimulieren, mehr GH zu produzieren, jeweils über leicht unterschiedliche, aber komplementäre Mechanismen.
CJC-1295 imitiert ein natürliches Signal des Gehirns, das der Hypophyse mitteilt, mehr Wachstumshormon zu produzieren, und verlängert sowie verstärkt diesen Effekt im Vergleich zu dem, was der Körper selbst leisten kann. Ipamorelin wirkt ähnlich, jedoch selektiver. Es stimuliert die Freisetzung von GH, ohne andere Hypophysenhormone wie Cortisol oder Prolaktin zu beeinflussen. Ihre Kombination wird häufig untersucht, da sich ihre Effekte gegenseitig verstärken können.
Warum ist Wachstumshormon für das Herz wichtig? Weil GH die Muskelmasse unterstützt, einschließlich des Myokards, das ebenfalls ein Muskel ist, den Fettstoffwechsel fördert und direkte Auswirkungen auf die Herzfunktion hat. Bei Patienten mit Herzinsuffizienz oder GH-Mangel sind niedrige Hormonspiegel mit einer schlechteren Prognose verbunden. Eine 2025 veröffentlichte Analyse auf DrOracle bestätigt, dass Ipamorelin sicherer ist als andere GH-Sekretagoga, da es nicht mit Cortisol oder Prolaktin interferiert, deren Anstieg erhebliche Nebenwirkungen verursachen kann.
Aus regulatorischer Sicht ist die Situation ähnlich wie bei den anderen diskutierten Peptiden: CJC-1295 und Ipamorelin haben keine zugelassenen Indikationen für die allgemeine Anwendung beim Menschen in der EU und werden ausschließlich als Forschungsstoffe vermarktet. Es gibt spezifische klinische Kontexte, in denen GH-Sekretion untersucht wird, aber die Standardisierung therapeutischer Protokolle für den Menschen ist derzeit unvollständig.
Endogene kardiale Peptide - vom Herzen produziert, um sich selbst zu schützen
Nicht alle für das Herz relevanten Peptide sind synthetische Substanzen aus Forschungslaboren. Einige werden direkt vom Herzen produziert, als eigenes Alarm- und Schutzsystem. B-Typ natriuretische Peptide (BNP, „brain natriuretic peptide“, trotz des Namens vom Herzen produziert) werden vom Myokard freigesetzt, wenn es überlastet ist. Ein Beispiel dafür ist die Herzinsuffizienz. Ihr erhöhter Blutspiegel dient als biologisches Alarmsignal und wird heute klinisch als diagnostischer Marker verwendet. Doch die Rolle von BNP ist nicht passiv: Es hemmt aktiv die Myokardfibrose (also die Umwandlung von Herzgewebe in starres Narbengewebe) und moduliert Entzündungen. Deshalb wirkt das Medikament Entresto, das bei Herzinsuffizienz eingesetzt wird, teilweise durch die Verstärkung der Effekte endogener natriuretischer Peptide.
Eine 2024 in Frontiers in Pharmacology veröffentlichte Übersicht, "Peptides Are Cardioprotective Drugs of the Future", analysiert ein breites Spektrum von Peptiden mit kardioprotektivem Potenzial und kommt zu dem Schluss, dass sich die kardiovaskuläre Medizin klar in Richtung Therapien entwickelt, die natürliche Schutzmechanismen des Herzens nachahmen oder verstärken, einschließlich synthetischer Peptide, die aktive biologische Sequenzen imitieren.
Orale Peptide: eine biologische Herausforderung und ein reales Versprechen
Oft wünschen sich Patienten eine einfach anzuwendende Therapie, die in den meisten Fällen eine Tablette ist. Leider ist diese Einfachheit bei der Behandlung mit Peptiden eingeschränkt. Das grundlegende Problem besteht darin, dass der Magen ein Peptid wie jedes andere Protein aus der Nahrung behandelt, nämlich indem er es in seine einzelnen Aminosäuren zerlegt. Eine BPC-157-Tablette zum Beispiel gelangt in den Magen, wird durch Verdauungsenzyme aufgelöst und gelangt nicht als aktives Peptid, sondern als einfache Aminosäuren ins Blut, die offensichtlich nicht die gleiche Wirkung haben.
Dennoch gibt es orale Peptide mit dokumentierten kardiovaskulären Effekten, insbesondere aus Nahrungsquellen. Ein von der Europäischen Union finanziertes Forschungsprogramm, das BACCCHUS-Projekt (CORDIS), hat gezeigt, dass bioaktive Peptide aus Lebensmitteln wie Fisch, Eiweiß, Weizen oder luftgetrocknetem Schinken zur Senkung des Blutdrucks beitragen, das Lipidprofil verbessern und die Produktion von Stickstoffmonoxid (dem oben erwähnten natürlichen Vasodilatator) erhöhen können, mit messbaren positiven Effekten in randomisierten kontrollierten Studien am Menschen.
Die moderne Pharmakologie entwickelt sich auch in Richtung spezieller Formulierungen, die synthetische Peptide vor der Verdauung schützen, wie Nanopartikel, Liposomen oder gleichzeitig verabreichte Enzyminhibitoren. Orales Semaglutid (die Tablettenform von Ozempic), bereits in der EU für Diabetes und Gewichtsmanagement zugelassen, zeigt, dass diese Barriere überwunden werden kann, auch wenn der Weg für andere Moleküle noch lang ist.

Topische Peptide: die zugänglichsten und mit den solidesten Nachweisen beim Menschen
Die direkte Anwendung auf der Haut ist der einfachste Weg zur Verabreichung von Peptiden und überraschenderweise der Bereich mit den meisten bereits validierten klinischen Anwendungen. Kosmetische Peptide haben es in weniger als zwei Jahrzehnten aus der Nische biochemischer Labore in die tägliche Pflegeroutine von Millionen Menschen geschafft.
Warum funktioniert der topische Weg für Peptide, obwohl wir gesehen haben, dass der orale Weg große Einschränkungen hat? Peptide mit kleinem Molekül können die Hornschicht, also die oberflächliche Hautschicht, durchdringen und die Dermis erreichen, die tiefere Schicht, in der sich die Fibroblasten befinden. Fibroblasten sind die Fabrikzellen der Haut: Sie produzieren Kollagen, Elastin und Hyaluronsäure, also genau die Moleküle, die für Festigkeit, Elastizität und Feuchtigkeit verantwortlich sind. Dort liefern Peptide für die Haut präzise biologische Botschaften: „produziere mehr Kollagen“, „bilde neue Gefäße“, „repariere die Hautbarriere“, „beruhige Entzündungen“. Gealterte oder geschädigte Haut erhält diese Anweisungen nicht in ausreichender Menge, und topische Peptide führen sie von außen wieder zu.
Matrixyl (Palmitoyl Pentapeptid-4), das Referenz-Anti-Aging-Peptid
Matrixyl ist wahrscheinlich das am besten erforschte Anti-Aging-Kosmetikpeptid der Welt. Sein Handelsname wird für Palmitoyl Pentapeptid-4 verwendet, ein synthetisches Molekül, das so entwickelt wurde, dass es Fragmente von abgebautem Kollagen nachahmt. Dadurch täuscht es der Haut vor, dass Kollagen beschädigt ist, um sie dazu anzuregen, als Ausgleich neues Kollagen zu produzieren.
Die klinischen Studien zu Matrixyl sind konsistent: Eine Formulierung auf Basis von Palmitoyl Pentapeptid-4 zeigte nach 8–12 Wochen täglicher Anwendung eine Verringerung der Faltentiefe um bis zu 45 % im Vergleich zur Placebogruppe, laut den von Peptide Journal zusammengefassten Daten. L'Oréal Paris, einer der größten Kosmetikhersteller der Welt, zitiert eine Studie, die zeigt, dass Peptide bei topischer Anwendung die Kollagenproduktion in der Haut um bis zu 30 % steigern können, mit sichtbaren Effekten bei der Reduzierung von Falten und der Verbesserung der Festigkeit. Matrixyl 3000, eine verbesserte Variante, die Palmitoyl Tetrapeptid-7 mit Palmitoyl Oligopeptid kombiniert, hat vergleichbare oder bessere Ergebnisse gezeigt, mit zusätzlichen Vorteilen bei der Reduzierung chronischer niedriggradiger Entzündungen, die mit der Hautalterung verbunden sind.
Aus mechanistischer Sicht: Matrixyl wirkt nicht direkt auf Falten, sondern baut die Struktur wieder auf, deren Symptom die Falten sind. Dies ist ein grundlegend anderer Ansatz als klassische Feuchtigkeitscremes, die die Haut vorübergehend aufpolstern, oder Filler-Behandlungen, die von außen Volumen hinzufügen. Matrixyl überzeugt die Haut, ihre eigenen Stützstrukturen wiederherzustellen.
Argireline (Acetyl Hexapeptid-3) — die kosmetische Alternative zu Botox
Argireline wird oft als „Botox in Cremeform“ bezeichnet, ein Vergleich, der vereinfacht, aber nicht völlig falsch ist. Der Mechanismus ist ähnlich: Botox blockiert die Freisetzung von Acetylcholin (der chemischen Substanz, mit der Nerven den Muskeln signalisieren, sich zusammenzuziehen) und lähmt dadurch vorübergehend die Gesichtsmuskeln, die Mimikfalten erzeugen. Argireline wirkt über einen ähnlichen, aber sanfteren Mechanismus: Es greift in den SNARE-Komplex ein, also in den molekularen Mechanismus, über den Neuronen Neurotransmitter freisetzen, und reduziert dadurch teilweise die Intensität der Kontraktionen der Gesichtsmuskeln, ohne die lähmende Wirkung des Botulinumtoxins.
Eine randomisierte, placebokontrollierte Studie, veröffentlicht im International Journal of Cosmetic Science, "A synthetic hexapeptide (Argireline) with antiwrinkle activity", zeigte, dass Argireline ein nicht-toxisches Peptid mit einer mechanisch mit Botulinumtoxin vergleichbaren Anti-Falten-Wirkung ist, jedoch ohne Neurotoxizität. Eine zweite klinische Studie, veröffentlicht in Skin Research and Technology, "The anti-wrinkle efficacy of argireline", untersuchte 60 Probanden, die Argireline vier Wochen lang zweimal täglich auf periokuläre Falten (die um die Augen) auftrugen. Ergebnis: 48,9 % der behandelten Gruppe zeigten eine Verbesserung der Falten im Vergleich zu 0 % in der Placebogruppe, mit einer signifikanten Reduktion objektiv gemessener Rauheitsparameter.
Der Vorteil gegenüber Botulinumtoxin ist offensichtlich: Argireline wird zu Hause aufgetragen, ohne Injektionen, ohne das Risiko asymmetrischer Lähmungen und ohne die Kosten wiederholter medizinischer Verfahren. Der Nachteil ist ebenso real: Die Effekte sind moderater und verschwinden nach Absetzen der Anwendung, Argireline baut die Hautstruktur nicht wieder auf, sondern reduziert vorübergehend die Muskelkontraktionen, die Mimikfalten vertiefen. Die besten Kandidaten für dieses Peptid sind Menschen mit Mimikfalten (Stirn, Augenwinkel, perioraler Bereich), nicht mit Falten, die durch Kollagenverlust oder langanhaltende Sonneneinstrahlung verursacht wurden.
Orale hydrolysierte Kollagenpeptide — was die interne Supplementierung bringt
Über die direkte topische Anwendung hinaus haben oral verabreichte Kollagenpeptide in den letzten Jahren enorm an Popularität gewonnen, und im Unterschied zu anderen oralen Peptiden gibt es hier tatsächlich klinische Studien am Menschen, die diese Popularität teilweise stützen. Hydrolysiertes Kollagen (also Kollagen, das in kleine, resorbierbare Peptide aufgespalten wurde) hat in mehreren randomisierten kontrollierten Studien messbare Vorteile für die Haut gezeigt.
Eine klinische Studie mit 105 Frauen im Alter zwischen 24 und 50 Jahren, die sechs Monate lang Kollagenpeptide konsumierten, dokumentierte bei allen Teilnehmerinnen eine glattere, elastischere Haut mit sichtbar verbessertem Erscheinungsbild. Studien mit hydrolysiertem PEPTAN-Kollagen zeigten, dass nach 12 Wochen Supplementierung die Kollagendichte in der Dermis im Vergleich zur Placebogruppe, bei der keine Veränderung festgestellt wurde, um 8,83 % zunahm. Warum funktioniert orales Kollagen, obwohl wir gesagt haben, dass Peptide im Magen abgebaut werden? Gerade weil hydrolysierte Kollagenpeptide bereits in kleine Fragmente, Dipeptide und Tripeptide vorverdaut sind, die relativ intakt über die Darmschleimhaut aufgenommen werden und in den Kreislauf gelangen, wo sie die Fibroblasten in der Dermis dazu anregen, eigenes Kollagen zu produzieren.
GHK-Cu — das Kupferpeptid mit drei Jahrzehnten Forschung
GHK-Cu (Glycyl-L-Histidyl-L-Lysin-Kupfer) ist eines der am besten erforschten topischen Peptide in der Geschichte der Biochemie. Es ist ein Tripeptid, also ein Peptid, das nur aus drei Aminosäuren besteht, und kommt natürlicherweise im Blutplasma junger Menschen vor. Mit 20 Jahren liegt sein Blutspiegel bei etwa 200 ng/mL; mit 60 Jahren sinkt er auf 80 ng/mL. Forscher haben beobachtet, dass dieser Rückgang mit dem altersbedingten Verlust der Fähigkeit zur Geweberegeneration zusammenfällt.
Eine 2018 im International Journal of Molecular Sciences veröffentlichte Studie, "Regenerative and Protective Actions of the GHK-Cu Peptide", dokumentierte, dass GHK-Cu das Wachstum von Blutgefäßen und Nerven stimuliert, die Produktion von Kollagen und Elastin erhöht, Entzündungen reduziert und das antioxidative System des Gewebes aktiviert. Darüber hinaus zeigte eine kontrollierte klinische Studie mit 71 Frauen, dass eine 12 Wochen lang angewendete Gesichtscreme mit GHK-Cu die Dichte und Dicke der Dermis erhöhte, Falten reduzierte und die Hauttextur verbesserte, mit Ergebnissen, die bei der Kollagenproduktion besser waren als Vitamin C oder Retinsäure.
Topisches Thymosin Beta-4 — das Peptid für die Heilung schwieriger Wunden
Thymosin Beta-4, topisch direkt auf eine Wunde oder Hautläsion aufgetragen, hat in Forschungsmodellen bemerkenswerte Effekte gezeigt. Eine 2024 im Journal of Tissue Engineering veröffentlichte Studie, "Discovery of Bioactive Peptides as Therapeutic Agents for Skin Wound Repair", dokumentiert, dass TB-4 die Re-Epithelisierung (also die Bedeckung der Wunde mit neuer Haut) und die lokale Angiogenese erhöht hat, mit einer besonders starken Aktivität bei der Stimulierung der Migration reparativer Zellen in den verletzten Bereich. Dies ist eine wertvolle Eigenschaft für chronische Wunden wie diabetische Ulzera, Dekubitus oder Wunden nach Bestrahlung, die ein großes klinisches Problem darstellen, bei dem die derzeitigen therapeutischen Optionen begrenzt sind.
Forschungspeptide: vielversprechend im Labor, derzeit nicht für die Anwendung beim Menschen zugelassen
Es ist an der Zeit, einen Aspekt zu klären, den das Internet oft mehrdeutig behandelt: den rechtlichen und medizinischen Status vieler der oben diskutierten Peptide.
In der Europäischen Union darf eine Substanz Menschen als Arzneimittel nur dann verabreicht werden, wenn sie eine Zulassung der EMA (Europäische Arzneimittel-Agentur) erhalten hat, nachdem sie klinische Studien der Phase I, II und III durchlaufen hat, die sowohl Sicherheit als auch Wirksamkeit nachweisen. Peptide wie BPC-157, TB-500, CJC-1295 oder Ipamorelin besitzen diese Zulassung nicht. Sie dürfen rechtlich als „Forschungsstoffe“ hergestellt und verkauft werden, was bedeutet, dass sie ausschließlich für das Labor und nicht für den menschlichen Konsum bestimmt sind.
Ein 2026 veröffentlichter Artikel über die Entwicklung des europäischen Peptidmarktes zeigt, dass die europäischen Behörden die Überwachung von Unternehmen intensiviert haben, die diese Stoffe als „research only“ (nur zu Forschungszwecken) kennzeichnen, sie aber offensichtlich für den menschlichen Konsum bewerben. Das ist ein reales Problem: Das Fehlen einer Regulierung bedeutet, dass Reinheit, exakte Konzentration und das Fehlen von Verunreinigungen von keiner Zertifizierungsstelle garantiert werden.
Der richtige Umgangston gegenüber diesen Molekülen ist weder totale Ablehnung noch unkritische Begeisterung. Ihre Erforschung ist vielversprechend und verdient es, fortgesetzt zu werden. Doch derzeit birgt ihre Anwendung am Menschen außerhalb eines kontrollierten Forschungsprotokolls unbekannte Risiken. Ein verantwortungsbewusster Arzt kann ihre Verwendung in der klinischen Standardpraxis gerade wegen des Fehlens vollständiger klinischer Nachweise am Menschen nicht empfehlen.
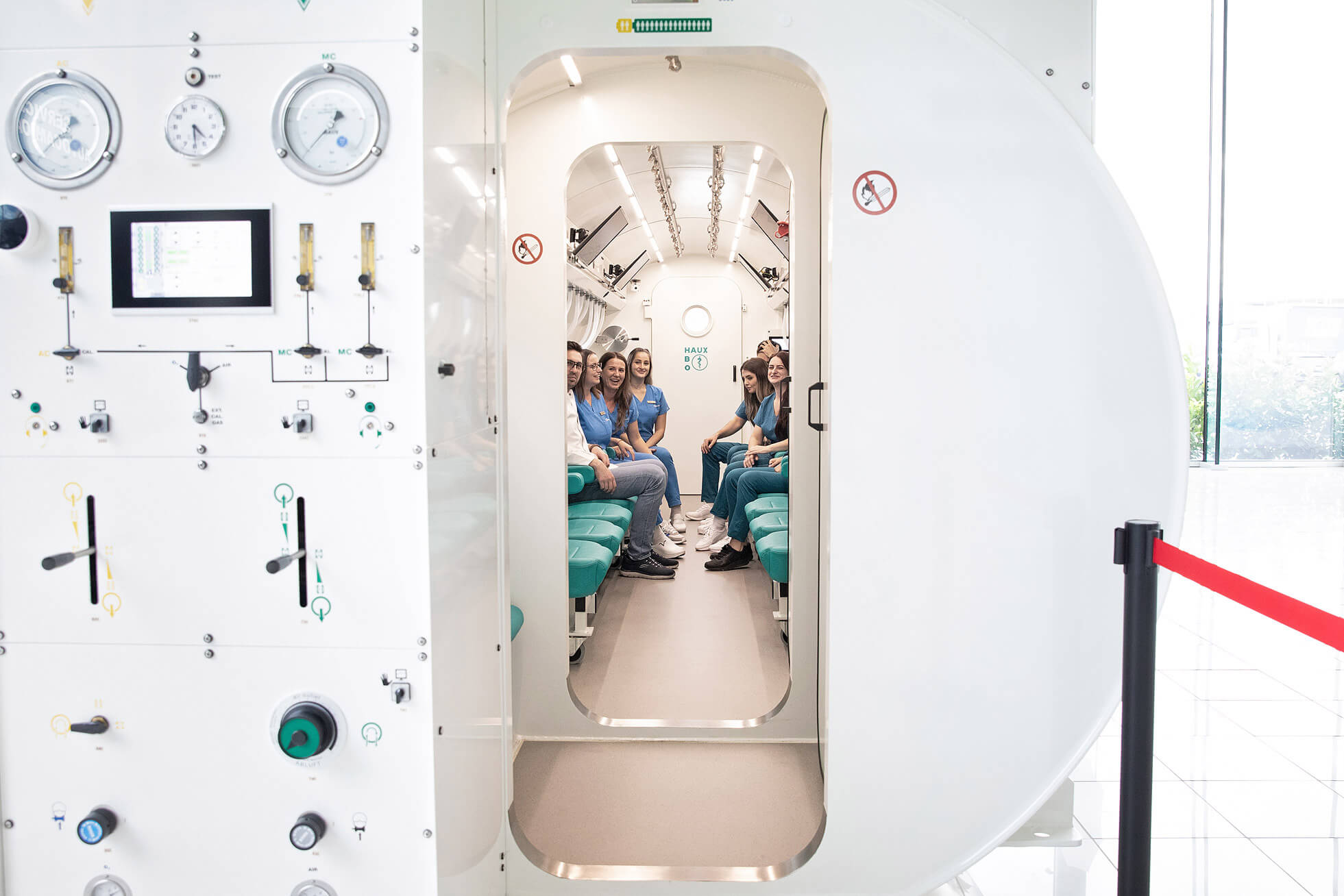
Wie die hyperbare Therapie die natürliche Peptidproduktion im Körper stimuliert
Es gibt einen Weg, über den die biologischen Mechanismen regenerativer Peptide ohne die Risiken eines nicht zugelassenen Produkts genutzt werden können: durch die Stimulierung ihrer Produktion durch den eigenen Organismus. Die medizinische hyperbare Therapie macht genau das und stützt sich dabei auf jahrzehntelange klinische Evidenz am Menschen.
Wenn ein Patient eine hyperbare Kammer betritt und 100 % Sauerstoff bei einem Druck einatmet, der zwei- bis dreimal höher ist als normal, erhält der Körper keine chemische Substanz von außen. Er erhält ein präzises physikalisches Signal, auf das er reagiert, indem er selbst die Moleküle produziert, die er zur Reparatur benötigt. VEGF, der Faktor, der die Bildung neuer Blutgefäße in ischämischen Bereichen steuert. BDNF, der Faktor, der Neuronen nach einem Schlaganfall oder einer neurologischen Verletzung ernährt und schützt. SDF-1, das Molekül, das wie ein Navigationssystem für Stammzellen funktioniert und sie aus dem Knochenmark genau an die verletzte Stelle ruft. All dies sind endogene Peptide und Wachstumsfaktoren, also vom Körper produzierte und nicht von außen eingeführte Stoffe.
Was aus Sicht der Peptidforschung bemerkenswert ist: Genau diese Moleküle versuchen Wissenschaftler synthetisch im Labor nachzubilden. BPC-157 stimuliert VEGF. TB-500 mobilisiert Vorläuferzellen in verletzte Bereiche, ähnlich wie SDF-1. CJC-1295 aktiviert eine hormonelle Kaskade, die die Gewebereparatur unterstützt. Die hyperbare Therapie aktiviert all diese Prozesse gleichzeitig, nicht durch die Einführung externer Moleküle mit unklarem Status, sondern durch die Schaffung der Bedingungen, unter denen der Körper sie selbst produziert, in den Dosen, die er natürlich reguliert und unter kontinuierlicher medizinischer Überwachung. Sie ist keine Kompromissalternative zu synthetischen Peptiden. In vielerlei Hinsicht ist sie der ursprüngliche Mechanismus, den die Peptidwissenschaft nachzuahmen versucht.
Warum die hyperbare Therapie heute die sichere Wahl ist
Die Peptide, über die wir in diesem Artikel gesprochen haben, BPC-157, TB-500, CJC-1295, Ipamorelin, haben eines gemeinsam: Die Laborergebnisse sind vielversprechend, aber die Studien am Menschen sind noch unzureichend, sodass kein Arzt sie als Behandlung empfehlen kann. Das bedeutet nicht, dass die dahinterstehende Wissenschaft falsch ist. Es bedeutet einfach, dass der Weg von Tierversuchen zur sicheren Behandlung von Menschen lang, kostspielig und für viele dieser Moleküle noch nicht vollständig zurückgelegt ist. Bis dieser Weg abgeschlossen ist, bleiben sie für die Forschung bestimmte Substanzen, nicht für den menschlichen Konsum.
Die hyperbare Therapie befindet sich in einer völlig anderen Position. Sie ist weder eine Neuheit noch ein Versprechen, sondern eine medizinische Methode, die seit mehr als sechs Jahrzehnten in Krankenhäusern und Kliniken auf der ganzen Welt eingesetzt wird, mit Hunderten von Studien an realen menschlichen Patienten und mit Protokollen, die von europäischen und internationalen medizinischen Organisationen offiziell anerkannt sind. Ein 2025 in PMC veröffentlichter Übersichtsartikel, "Application and Progress of Hyperbaric Oxygen Therapy in Cardiovascular Diseases", dokumentiert, dass die hyperbare Therapie den Herzmuskel nach einem Infarkt schützt, die Bildung neuer Blutgefäße in betroffenen Bereichen stimuliert und die Fähigkeit der Gefäße verbessert, normal zu funktionieren. All dies sind beim Menschen gemessene Effekte, nicht nur Ergebnisse aus Tierversuchen.
Auch bei der Erholung nach einem Schlaganfall sind die Ergebnisse ebenso klar. Eine 2013 in PLOS ONE veröffentlichte Studie, "Hyperbaric Oxygen Induces Late Neuroplasticity in Post Stroke Patients", zeigte etwas Bemerkenswertes: Patienten mit neurologischen Defiziten, die zwei Jahre nach einem Schlaganfall noch bestanden, also in einer Phase, in der sich das Gehirn nicht mehr spontan erholt, zeigten nach 40 Sitzungen hyperbarer Therapie reale Verbesserungen. Darüber hinaus war auf Gehirnaufnahmen zu sehen, dass Bereiche des Gehirns, die nicht mehr funktionierten, „reaktiviert“ wurden. Dies nennt man Neuroplastizität, die Fähigkeit des Gehirns, neue Verbindungen zu bilden, und sie ist praktisch die Grundlage jeder neurologischen Erholung.
Ein weiterer konkreter Vorteil der hyperbaren Therapie ist, dass man genau weiß, was man erhält. Laut StatPearls / NIH sind die „Hyperbaric Cardiovascular Effects“ der hyperbaren Therapie gut dokumentiert und reproduzierbar: Sauerstoff löst sich in bis zu 20-fach höheren Mengen als normal im Blut und erreicht Gewebe sogar dort, wo die Durchblutung schlecht ist, mit gut charakterisierten entzündungshemmenden und regenerationsfördernden Effekten. In einer zertifizierten medizinischen Klinik wie Hyperbarium findet jede Sitzung mit 100 % Sauerstoff, unter standardisiertem Druck, mit geprüften Geräten und unter kontinuierlicher medizinischer Überwachung statt. Es gibt keine Überraschungen hinsichtlich Produktqualität oder Dosis, reale Probleme bei online gekauften Forschungspeptiden, bei denen niemand garantiert, dass die Ampulle genau das enthält, was auf dem Etikett steht.
Die Zukunft der Peptide: wohin sich die Forschung entwickelt
Die Forschung zu therapeutischen Peptiden befindet sich in den Jahren 2025–2026 an einem interessanten Punkt. Wir sind nicht mehr in der Phase, in der Wissenschaftler gerade erst entdecken, dass diese Moleküle existieren und bemerkenswerte Dinge tun können.
Einige Moleküle befinden sich bereits in klinischen Studien der Phase I und II, das heißt, sie werden erstmals an Menschen in kleinen Gruppen von Freiwilligen getestet, um Sicherheit und optimale Dosierung zu bewerten. Andere befinden sich in der Phase der Optimierung ihrer Formulierung: Forscher suchen nach Lösungen, um sie stabil, resorbierbar und bequem verabreichbar zu machen, ohne dass sie ihre biologische Aktivität verlieren. Eine 2025 in Biomolecules veröffentlichte Studie, "Bioactive peptides: from preclinical to clinical studies", identifiziert mehrere prioritäre Richtungen: Peptide, die bei der Kontrolle des Cholesterins helfen, Peptide mit direkter entzündungshemmender Wirkung auf Blutgefäße und Peptide, die hormonelle Systeme mit breiter metabolischer Wirkung modulieren. All dies sind Bereiche, in denen weit verbreitete chronische Krankheiten wie Herz-Kreislauf-Erkrankungen, Diabetes und Adipositas dringend neue Lösungen benötigen.
Im Bereich der Hautpflege ist der Fortschritt bereits sichtbar. Neue Varianten von GHK-Cu und Peptiden der extrazellulären Matrix werden für fortschrittliche medizinische Formulierungen jenseits der Kosmetik untersucht, zur Behandlung chronischer Wunden, pathologischer Narben und entzündlicher dermatologischer Erkrankungen. In der Onkologie stellen antimikrobielle Peptide und Peptide der Immun-Signalübertragung eine aktive Grenze dar, wobei einige Moleküle bereits in klinischen Studien für bestimmte Krebsarten untersucht werden. In der Neurologie werden neurotrophe Peptide, also Moleküle, die Neuronen nähren und schützen, als potenzielle Werkzeuge bei Alzheimer, Parkinson und der posttraumatischen Erholung untersucht.
Es gibt auch ein strukturelles Hindernis, das die Peptidforschung überwinden muss: Viele der vielversprechendsten Verbindungen können nicht patentiert werden, weil sie aus natürlichen biologischen Sequenzen abgeleitet sind. Ohne Patent haben Pharmaunternehmen geringere finanzielle Anreize, Hunderte Millionen Euro in vollständige klinische Studien zu investieren. Dies ist paradoxerweise einer der Gründe, warum einige Peptide mit ausgezeichneten präklinischen Ergebnissen jahrelang im Forschungsbereich bleiben, nicht weil die Wissenschaft schwach wäre, sondern weil das ökonomische Modell der klinischen Forschung Moleküle nicht begünstigt, die nicht das exklusive Eigentum eines Unternehmens werden können.
Was sicher ist: Peptide sind keine vorübergehende Modeerscheinung. Sie sind Teil der grundlegenden Biologie jedes lebenden Organismus, und das Verständnis dafür, wie sie therapeutisch genutzt werden können, wird sich weiterentwickeln. Einige werden zu zugelassenen Arzneimitteln werden. Andere bleiben im Bereich der Kosmetika und Nahrungsergänzungsmittel mit solider Evidenz. Und wieder andere, die komplexesten, werden noch einige Jahre warten müssen, bis klinische Studien am Menschen die Versprechen aus dem Labor bestätigen oder widerlegen. Bis dahin ist das Beste, was ein informierter Patient tun kann, den Unterschied zwischen Evidenz und Versprechen zu verstehen und jede therapeutische Entscheidung gemeinsam mit einem Arzt zu treffen, der sowohl das Potenzial als auch die Grenzen dieses faszinierenden Bereichs kennt.




