
Articol revizuit de: Dr. Sturz Ciprian, Dr. Tîlvescu Cătălin și Dr. Alina Vasile
Articol actualizat la data: 04-04-2026
Tot ce trebuie să știi despre peptide: de la știința regenerării la protocoale de cercetare
- Ce sunt peptidele?
- De ce interesează peptidele medicina cardiovasculară
- Peptide injectabile: cele mai cercetate și cele mai discutate
- Peptide orale: o provocare biologică și o promisiune reală
-
Peptide topice: cele mai accesibile și cu cele mai solide dovezi la om
- Matrixyl (Palmitoil Pentapeptida-4), peptida de referință anti-aging
- Argireline (Acetil Hexapeptida-3) — alternativa cosmetică la botox
- Peptide de colagen hidrolizat oral — ce aduce suplimentarea internă
- GHK-Cu — peptida cu cupru și trei decenii de studii
- Thymosin Beta-4 topic — peptida care se ocupă de vindecarea plăgilor dificile
- Peptidele de cercetare: promițătoare în laborator, necertificate deocamdată pentru uz uman
- Cum stimulează terapia hiperbară producția naturală de peptide în corp
- De ce terapia hiperbară este alegerea sigură astăzi
- Viitorul peptidelor: unde se îndreaptă cercetarea
Dacă ai auzit recent despre peptide, la cabinet, pe internet sau dintr-un podcast despre longevitate, și te-ai întrebat ce sunt, dacă funcționează cu adevărat și dacă sunt sigure, ești în locul potrivit. Peptidele au devenit unul dintre subiectele cel mai mult discutate în medicina modernă, și nu fără motiv. Cercetătorii descoperă că aceste molecule minuscule, pe care corpul nostru le produce în mod natural, au un potențial regenerativ remarcabil, de la vindecarea țesuturilor și sănătatea inimii, până la recuperarea după un accident vascular cerebral.
Dar înainte de orice entuziasm, este important să înțelegi exact ce știm, ce nu știm încă și unde se află granița dintre promisiune și realitate clinică. Acest articol îți explică tot: tipurile de peptide, ce spun studiile medicale, cum se folosesc și, spre final, de ce terapia hiperbară medicală rămâne, deocamdată, una dintre cele mai sigure și mai bine documentate opțiuni pentru sănătatea inimii și a creierului.
Ce sunt petidele?
Gândește-te la proteinele din corpul tău ca la niște lanțuri lungi de zale. Fiecare za este un aminoacid. O peptidă este, practic, un fragment scurt dintr-un astfel de lanț, adică câteva zale legate împreună, de obicei între 2 și 50 de aminoacizi. Atunci când lanțul devine mai lung de 50, vorbim deja despre o proteină.
Ce face peptidele speciale nu este dimensiunea lor mică, ci precizia cu care acționează. Fiecare peptidă se potrivește ca o cheie într-o lacăt specific, un receptor de pe suprafața celulelor, și transmite un mesaj precis: „construiește colagen", „formează vase noi de sânge", „reduce inflamația", „repară țesutul lezat". Corpul uman produce sute de astfel de mesageri în mod natural. Insulina este o peptidă. Oxitocina este o peptidă. Hormonul de creștere acționează prin peptide. Ideea din spatele terapiei cu peptide este simplă: dacă aceste molecule există deja în organism și fac lucruri bune, putem oare să le folosim sau să le stimulăm terapeutic?
Răspunsul cercetării este: da, dar cu multă nuanță.
De ce interesează peptidele medicina cardiovasculară
Sistemul cardiovascular este, probabil, domeniul în care peptidele au demonstrat cel mai mare potențial regenerativ. Motivul este simplu: inima este un organ cu o capacitate extrem de redusă de autoregenerare. Dacă rinichiul sau ficatul pot compensa până la un punct, inima nu poate înlocui eficient celulele musculare pierdute după un infarct. Tocmai acolo intră în discuție peptidele, ca potențiali „arhitecți" ai unui proces de regenerare pe care corpul singur nu îl poate completa.
Iar contextul epidemiologic face ca această discuție să fie urgentă. Conform Institutului Național de Sănătate Publică, bolile cardiovasculare sunt responsabile pentru aproape 56% din totalul deceselor înregistrate în România. Potrivit datelor Ministerului Sănătății, rata mortalității cardiovasculare din România este de 2,5 ori mai mare decât media Uniunii Europene.
Iar hipertensiunea arterială, unul dintre principalii factori de risc, afectează peste 45% din adulții din România, potrivit Societății Române de Hipertensiune Arterială. Cifrele acestea nu sunt statistici abstracte. Ele descriu o criză de sănătate publică în care orice nouă opțiune terapeutică merită luată în serios.
Peptide injectabile: cele mai cercetate și cele mai discutate
Peptidele injectabile sunt categoria cu cel mai mare volum de cercetare și, totodată, cu cel mai mult interes din partea publicului informat. Motivul pentru care se preferă injectarea față de înghițirea unei pastile este simplu: stomacul nostru descompune peptidele ca pe orice altă proteină. Enzimele digestive le mărunțesc în bucăți, înainte ca molecula activă să ajungă în sânge. Administrarea injectabilă subcutanată (sub piele) sau intramusculară ocolește această problemă și permite peptidei să ajungă direct în circulație, intactă.
BPC-157 — peptida din sucul gastric
Dacă ar fi să alegi o singură peptidă care a generat cel mai mare val de interes în cercetarea medicală a ultimului deceniu, aceea ar fi, aproape sigur, BPC-157. Nu pentru că ar fi cea mai spectaculoasă ca denumire, prescurtarea vine de la „Body Protective Compound 157", adică compusul protector 157 al organismului, ci pentru că spectrul efectelor documentate în studii este neobișnuit de larg pentru o moleculă atât de mică.
Originea ei este, la prima vedere, surprinzătoare: este o secvență de 15 aminoacizi derivată dintr-o proteină prezentă natural în sucul gastric uman. Stomacul nostru o produce în mod constant, iar cercetătorii au observat de-a lungul timpului că tractul digestiv are o capacitate remarcabilă de a se vindeca rapid după leziuni. Întrebarea firească a fost: oare BPC-157 are legătură cu această capacitate? Și dacă da, poate fi folosită în alte țesuturi?
Răspunsul cercetărilor de până acum este, cu precauțiile de rigoare, afirmativ. O analiză sistematică publicată în 2025 de cercetători de la Case Western Reserve University, apărută în HSS Journal, "Emerging Use of BPC-157 in Orthopaedic Sports Medicine", a trecut în revistă 544 de articole și a inclus 36 de studii. Concluzia? BPC-157 stimulează producția de VEGF (adică factorul de creștere al vaselor de sânge), activează căile de multiplicare celulară și reduce citokinele inflamatorii, adică moleculele care „întrețin" inflamația cronică. Tradus simplu: această peptidă pare să spună celulelor: construiți vase noi de sânge, înmulțiți-vă și opriți incendiul inflamator. Toate trei sunt procese cruciale după un infarct sau orice altă leziune a țesutului cardiac.
Un alt studiu publicat în 2025 în PMC, "Regeneration or Risk? A Narrative Review of BPC-157", confirmă că BPC-157 stimulează producția de oxid nitric, o moleculă pe care vasele de sânge o folosesc natural pentru a se dilata și a permite un flux mai bun. Când vasele produc prea puțin oxid nitric (ceea ce se întâmplă în ateroscleroză, diabet sau hipertensiune) sângele curge mai greu, tensiunea crește și riscul de infarct urcă. BPC-157 pare să poată reactiva acest tranzit natural.
Un studiu din 2025, "Protective Effects of BPC-157 on Liver, Kidney, and Lung Following Lower Extremity Ischemia-Reperfusion", a arătat că peptida a protejat ficatul, rinichii și plămânii de deteriorarea cauzată de lipsa de sânge și revenirea sa bruscă, un mecanism cunoscut drept „leziune de reperfuzie", despre care vom vorbi mai jos în contextul infarctului.
Toate acestea sună promițător. Și chiar sunt. Dar există o nuanță esențială pe care orice articol onest trebuie să o spună clar: BPC-157 nu este aprobat ca medicament în Uniunea Europeană sau de FDA pentru nicio indicație la om. Toate studiile menționate sunt realizate pe animale. BPC-157 este comercializat legal exclusiv ca substanță pentru cercetare, adică pentru uz în laborator, nu pentru consum uman. Profilul de siguranță pe termen lung la om este necunoscut. Dar, asta nu diminuează valoarea cercetării, dar înseamnă că decizia de utilizare nu poate fi luată fără supraveghere medicală atentă și fără înțelegerea clară a limitelor dovezilor actuale.
TB-500 și Thymosin Beta-4, semnalul de alarmă al vaselor de sânge
Există în organism un sistem de urgență biologic remarcabil: atunci când un țesut este lezat, celulele din jurul rănii emit semnale chimice care „cheamă" celule reparatoare din alte zone ale corpului, inclusiv din măduva osoasă, unde sunt stocate celulele stem. Thymosin Beta-4 este una dintre moleculele care coordonează această mobilizare. Este produsă natural de timus, o glandă imunitară situată în spatele sternului, aproximativ de dimensiunea uneismochine, și joacă un rol central în mobilizarea celulelor progenitoare endoteliale, adică acele celule „pre-vasculare" capabile să contribuie la refacerea vaselor de sânge deteriorate. TB-500 este o variantă sintetică a fragmentului ei activ, concepută pentru a reproduce această acțiune de mobilizare și reparare.
Un studiu publicat în 2024 în revista Angiogenesis, "Restoration of Blood Vessel Regeneration in the Era of Advanced Therapies", documentează că Thymosin Beta-4 stimulează migrarea celulelor endoteliale spre zonele deteriorate, reduce inflamația peretelui vascular și promovează formarea de noi capilare. Capilarele sunt cele mai mici vase de sânge din corp, o rețea invizibilă ochiului liber, dar esențială pentru că ea asigură hrănirea celulelor individuale. Când un infarct sau un AVC distruge această rețea fină, țesuturile nu mai primesc oxigen și glucoză, chiar dacă arterele mari sunt reperfuzate. Thymosin Beta-4 ar putea ajuta la reconstrucția acestei rețele fine, un efect pe care nicio altă terapie actuală nu îl adresează direct.
Un studiu publicat în PLOS ONE a demonstrat că TB-4 aplicat în modele experimentale a crescut re-epitelizarea plăgilor cu până la 61% față de grupul martor, cu o creștere semnificativă a depunerii de colagen și a angiogenezei locale. Stimularea migrării celulelor care acoperă și protejează pielea a fost de 2 până la 3 ori mai mare decât în grupul netratat, la doze extrem de mici, de ordinul picogramelor. Aceasta sugerează că TB-4 funcționează ca un semnal de amplitudine mică, dar cu efect biologic disproporționat față de cantitatea administrată.
La fel ca BPC-157, TB-500 este comercializat exclusiv pentru cercetare și nu are autorizare pentru utilizare terapeutică la om în UE sau SUA
CJC-1295 și Ipamorelin, peptidele care stimulează hormonul de creștere
Până acum am vorbit despre peptide care acționează direct asupra țesuturilor, adică a vaselor de sânge, mușchilor, pielii. Există însă o altă categorie de peptide cu un mecanism complet diferit: în loc să repare direct, ele activează hipofiza. Aceasta este o glandă mică la baza creierului, de dimensiunea unui bob de mazăre, care coordonează producția mai multor hormoni esențiali, inclusiv hormonul de creștere (GH). CJC-1295 și Ipamorelin sunt două peptide care stimulează hipofiza să producă mai mult GH, fiecare prin mecanisme ușor diferite, dar complementare.
CJC-1295 imită un semnal natural al creierului care transmite hipofizei să producă mai mult hormon de creștere, prelungind și amplificând efectul acestui semnal față de ce poate produce corpul singur. Ipamorelin face același lucru, dar cu o selectivitate mai mare. El stimulează eliberarea de GH fără să perturbe alți hormoni hipofizari, cum ar fi cortizolul sau prolactina. Combinarea lor este frecvent studiată tocmai pentru că efectele se potențează reciproc.
De ce contează hormonul de creștere pentru inimă? Pentru că GH sprijină masa musculară, inclusiv miocardul, care este și el un mușchi, favorizează metabolismul grăsimilor și are efecte directe asupra funcției cardiace. La pacienții cu insuficiență cardiacă sau cu deficiență de GH, nivelurile scăzute ale acestui hormon sunt asociate cu un prognostic mai prost. O analiză din 2025 publicată pe DrOracle confirmă că Ipamorelin este mai sigur decât alți secretagogi ai GH tocmai pentru că nu interferă cu cortizolul sau cu prolactina, hormoni a căror creștere poate genera efecte adverse semnificative.
Din punct de vedere regulatoriu, situația este similară celorlalte peptide discutate: CJC-1295 și Ipamorelin nu au indicații aprobate pentru utilizare generală la om în UE și sunt comercializate exclusiv ca substanțe de cercetare. Există contexte clinice specifice în care secrețiile de GH sunt studiate, dar standardizarea protocoalelor terapeutice umane este, deocamdată, incompletă.
Peptidele cardiace endogene - produse de inima pentru a se proteja singură
Nu toate peptidele relevante pentru inimă sunt substanțe sintetice din laboratoare de cercetare. Unele sunt produse chiar de inimă, ca sistem propriu de alarmă și protecție. Peptidele natriuretice de tip B (BNP adică brain natriuretic peptide, în ciuda numelui, produse de inimă) sunt eliberate de miocard atunci când acesta este suprasolicitat. Un exemplu în acest sens este insuficiența cardiacă. Nivelul lor crescut în sânge funcționează ca un semnal de alarmă biologic și este folosit astăzi în clinică ca marker de diagnostic. Dar rolul BNP nu este pasiv: el inhibă activ fibroza miocardică (adică transformarea țesutului cardiac în cicatrice rigidă) și modulează inflamația. Tocmai de aceea, medicamentul Entresto, aprobat pentru insuficiența cardiacă, funcționează parțial prin amplificarea efectelor peptidelor natriuretice endogene.
O sinteză publicată în 2024 în Frontiers in Pharmacology, "Peptides Are Cardioprotective Drugs of the Future", analizează un spectru larg de peptide cu potențial cardioprotector și concluzionează că medicina cardiovasculară se îndreaptă clar spre terapii care mimează sau potențează mecanismele biologice naturale de protecție cardiacă, inclusiv prin peptide sintetice proiectate să imite secvențe biologice active.
Peptide orale: o provocare biologică și o promisiune reală
De multe ori, pacienții cer tratamentul simplu de gestionat, care în cele mai multe cazuri este o pastilă. Din păcate, când vine vorba de tratamentul cu peptide această simplicitate este nuanțată. Problema fundamentală este că stomacul tratează o peptidă la fel ca pe orice altă proteină din mâncare, adică o descompune în aminoacizii ei individuali. O pastilă cu BPC-157, de exemplu, ajunge în stomac, este dizolvată de enzimele digestive și ajunge în sânge nu ca peptidă activă, ci ca aminoacizi simpli, care, în mod evident, nu mai au același efect.
Cu toate acestea, există peptide orale cu efect cardiovascular documentat, mai ales din surse alimentare. Un program de cercetare finanțat de Uniunea Europeană, Proiectul BACCCHUS (CORDIS), a demonstrat că peptidele bioactive din alimente precum peștele, albușul de ou, grâul sau șunca uscată pot contribui la scăderea tensiunii arteriale, la îmbunătățirea profilului lipidic și la creșterea producției de oxid nitric (cel vasodilatator natural menționat mai sus), cu efecte benefice măsurabile în studii randomizate controlate la om.
Farmacologia modernă avansează și în direcția unor formulări speciale care să protejeze peptidele sintetice de degradarea digestivă precum nanoparticule, liposomi sau inhibitori de enzime administrați simultan. Semaglutida orală (varianta comprimat a Ozempicului), deja aprobată în UE pentru diabet și management ponderal, demonstrează că această barieră poate fi depășită, chiar dacă drumul rămâne lung pentru alte molecule.

Peptide topice: cele mai accesibile și cu cele mai solide dovezi la om
Aplicarea directă pe piele este cea mai simplă cale de administrare a peptidelor, și, în mod surprinzător, domeniul cu cele mai multe aplicații clinice deja validate. Peptidele cosmetice au trecut în mai puțin de două decenii din nișa laboratoarelor de biochimie în rutina zilnică de îngrijire a milioane de oameni.
De ce funcționează calea topică pentru peptide, deși am văzut că cea orală are limitări majore? Peptidele cu moleculă mică pot penetra stratul cornos, adică stratul superficial, al pielii și ajunge în dermă, stratul profund unde se află fibroblastele. Fibroblastele sunt celulele-uzine ale pielii: ele produc colagen, elastină și acidul hialuronic, adică exact moleculele responsabile de fermitate, elasticitate și hidratare. Acolo, peptidele pentru piele livrează mesaje biologice precise: „produce mai mult colagen”, „formează vase noi”, „repară bariera cutanată”, „calmează inflamația”. Pielea îmbătrânită sau deteriorată nu primește aceste instrucțiuni în cantitate suficientă, iar peptidele topice le reintroduc din exterior.
Matrixyl (Palmitoil Pentapeptida-4), peptida de referință anti-aging
Matrixyl este, probabil, cea mai studiată peptidă cosmetică anti-aging din lume. Denumirea sa comercială este folosită pentru palmitoil pentapeptida-4, o moleculă sintetică proiectată să mimeze fragmentele de colagen degradat. Astfel, ea păcălește pielea că are colagen rupt, pentru a o stimula să producă colagen nou în compensație.
Studiile clinice pe Matrixyl sunt consistente: o formulare pe bază de palmitoil pentapeptidă-4 a demonstrat o reducere a adâncimii ridurilor de până la 45% față de grupul placebo, după 8–12 săptămâni de utilizare zilnică, potrivit datelor sintetizate de Peptide Journal. L'Oréal Paris, unul dintre cei mai mari producători cosmetici din lume, citează un studiu care arată că peptidele pot stimula producția de colagen în piele cu până la 30% când sunt aplicate topic, cu efecte vizibile în reducerea ridurilor și îmbunătățirea fermității. Matrixyl 3000, o variantă îmbunătățită care combină palmitoil tetrapeptida-7 cu palmitoil oligopeptida, a demonstrat rezultate comparabile sau superioare, cu beneficii suplimentare în reducerea inflamației cronice de joasă intensitate, asociate îmbătrânirii pielii.
Din perspectiva mecanismului: Matrixyl nu acționează direct pe riduri, ci reconstruiește structura din care ridurile sunt simptomul. Acesta este un tip de abordare profund diferit față de hidratantele clasice, care umflă temporar pielea, sau față de procedurile de umplere, care adaugă volum din exterior. Matrixyl convinge pielea să-și refacă propriile structuri de susținere.
Argireline (Acetil Hexapeptida-3) — alternativa cosmetică la botox
Argireline este adesea denumită „botox în cremă", o comparație care simplifică, dar nu este complet greșită. Mecanismul este similar: botoxul blochează eliberarea acetilcolinei (substanța chimică prin care nervii comandă mușchilor să se contracte), paralizând temporar mușchii faciali care produc riduri de expresie. Argireline acționează printr-un mecanism similar, dar mai blând, interferă cu complexul SNARE, adică cu mecanismul molecular prin care neuronii eliberează neurotransmițători, reducând parțial intensitatea contracțiilor musculare faciale, fără efectul de paralizie al toxinei botulinice.
Un studiu randomizat, controlat cu placebo, publicat în International Journal of Cosmetic Science, "A synthetic hexapeptide (Argireline) with antiwrinkle activity", a demonstrat că Argireline este o peptidă non-toxică cu activitate antirid comparabilă mecanic cu a toxinei botulinice, dar fără neurotoxicitate. Un al doilea studiu clinic publicat în Skin Research and Technology, "The anti-wrinkle efficacy of argireline", a evaluat 60 de subiecți care au aplicat Argireline pe ridurile perioculare (cele din jurul ochilor) de două ori pe zi, timp de patru săptămâni. Rezultat: 48,9% din grupul tratat a prezentat îmbunătățire antirid față de 0% în grupul placebo, cu reducere semnificativă a parametrilor de rugozitate măsurați obiectiv.
Avantajul față de toxina botulinică este evident: Argireline se aplică acasă, fără injecții, fără risc de paralizie asimetrică și fără costul procedurilor medicale repetate. Dezavantajul, la fel de real: efectele sunt mai moderate și dispar odată cu întreruperea utilizării, Argireline nu reconstruiește structura pielii, ci reduce temporar contracțiile musculare care adâncesc ridurile de expresie. Cei mai buni candidați pentru această peptidă sunt persoanele cu riduri de expresie (fruntea, colțurile ochilor, zona periobuzală), nu cu riduri cauzate de pierderea de colagen sau de expunerea prelungită la soare.
Peptide de colagen hidrolizat oral — ce aduce suplimentarea internă
Dincolo de aplicarea topică directă, peptidele de colagen administrate oral au căpătat o popularitate uriașă în ultimii ani și, în mod excepțional față de alte peptide orale, există studii clinice pe oameni care susțin parțial această popularitate. Colagenul hidrolizat (adică colagen descompus în peptide mici, absorbabile) a demonstrat, în mai multe studii randomizate controlate, beneficii măsurabile asupra pielii.
Un studiu clinic realizat pe 105 femei cu vârste între 24 și 50 de ani, care au consumat peptide de colagen timp de șase luni, a documentat o piele mai netedă, mai elastică și cu aspect vizibil îmbunătățit la toate participantele. Studiile cu colagenul hidrolizat PEPTAN au arătat că, după 12 săptămâni de suplimentare, densitatea colagenului din dermă a crescut cu 8,83% față de grupul placebo, unde nu s-a înregistrat nicio modificare. De ce funcționează colagenul oral, deși am spus că peptidele se degradează în stomac? Tocmai pentru că peptidele de colagen hidrolizat sunt deja pre-digerate în fragmente mici, dipeptide și tripeptide care pot fi absorbite relativ intacte prin mucoasa intestinală și ajung în circulație, unde stimulează fibroblastele din derm să producă colagen propriu.
GHK-Cu — peptida cu cupru și trei decenii de studii
GHK-Cu (glicil-L-histidil-L-lizin-cupru) este una dintre cele mai studiate peptide topice din istoria biochimiei. Este o tripeptidă, adică o peptidă formată din doar trei aminoacizi, prezentă natural în plasma sanguină a oamenilor tineri. La 20 de ani, nivelul ei în sânge este de aproximativ 200 ng/mL; la 60 de ani, scade la 80 ng/mL. Cercetătorii au observat că această scădere coincide cu pierderea capacității de regenerare tisulară odată cu vârsta.
Un studiu publicat în International Journal of Molecular Sciences în 2018, "Regenerative and Protective Actions of the GHK-Cu Peptide", a documentat că GHK-Cu stimulează creșterea vaselor de sânge și a nervilor, crește producția de colagen și elastină, reduce inflamația și activează sistemul antioxidant tisular. Mai mult, un studiu clinic controlat cu 71 de femei a arătat că o cremă facială cu GHK-Cu aplicată 12 săptămâni a crescut densitatea și grosimea dermei, a redus ridurile și a ameliorat textura pielii, cu rezultate superioare vitamina C sau acidului retinoic în producerea de colagen.
Thymosin Beta-4 topic — peptida care se ocupă de vindecarea plăgilor dificile
Thymosin Beta-4, aplicată topic direct pe o plagă sau o leziune cutanată, a demonstrat efecte remarcabile în modele de cercetare. Un studiu publicat în 2024 în Journal of Tissue Engineering, "Discovery of Bioactive Peptides as Therapeutic Agents for Skin Wound Repair", documentează că TB-4 a crescut re-epitelizarea (adică acoperirea cu piele nouă a plăgii) și angiogeneza locală, cu o activitate deosebită în stimularea migrării celulelor reparatoare spre zona de leziune. Aceasta este o proprietate valoroasă pentru plăgile cronice precum ulcerele diabetice, escarele de decubit sau rănile post-iradiere, care reprezintă o problemă clinică majoră în care opțiunile terapeutice actuale sunt limitate.
Peptidele de cercetare: promițătoare în laborator, necertificate deocamdată pentru uz uman
Este momentul să clarificăm un aspect pe care internetul îl tratează adesea cu ambiguitate: statutul legal și medical al multor peptide discutate mai sus.
În Uniunea Europeană, o substanță poate fi administrată oamenilor ca medicament doar dacă a primit autorizare de la EMA (Agenția Europeană pentru Medicamente), după ce a parcurs studii clinice de faza I, II și III care demonstrează atât siguranța, cât și eficacitatea. Peptide precum BPC-157, TB-500, CJC-1295 sau Ipamorelin nu au această autorizare. Ele pot fi produse și vândute legal ca „substanțe pentru cercetare", ceea ce înseamnă că sunt destinate exclusiv laboratorului, nu consumului uman.
Un articol publicat în 2026 privind evoluția pieței europene de peptide arată că autoritățile europene au intensificat supravegherea companiilor care etichetează aceste substanțe drept „research only" (nr. doar în scop de cercetare), dar le promovează evident pentru consum uman. Aceasta este o problemă reală: lipsa reglementării înseamnă că puritatea, concentrația exactă și absența contaminanților nu sunt garantate de niciun organism de certificare.
Tonul corect față de aceste molecule nu este nici cel al respingerii totale, nici cel al entuziasmului necritic. Cercetarea lor este promițătoare și merită continuată. Dar, la ora actuală, administrarea lor umană în afara unui protocol de cercetare controlat implică riscuri necunoscute. Un medic responsabil nu poate recomanda utilizarea lor în practica clinică standard, tocmai din cauza absenței dovezilor clinice complete la om.
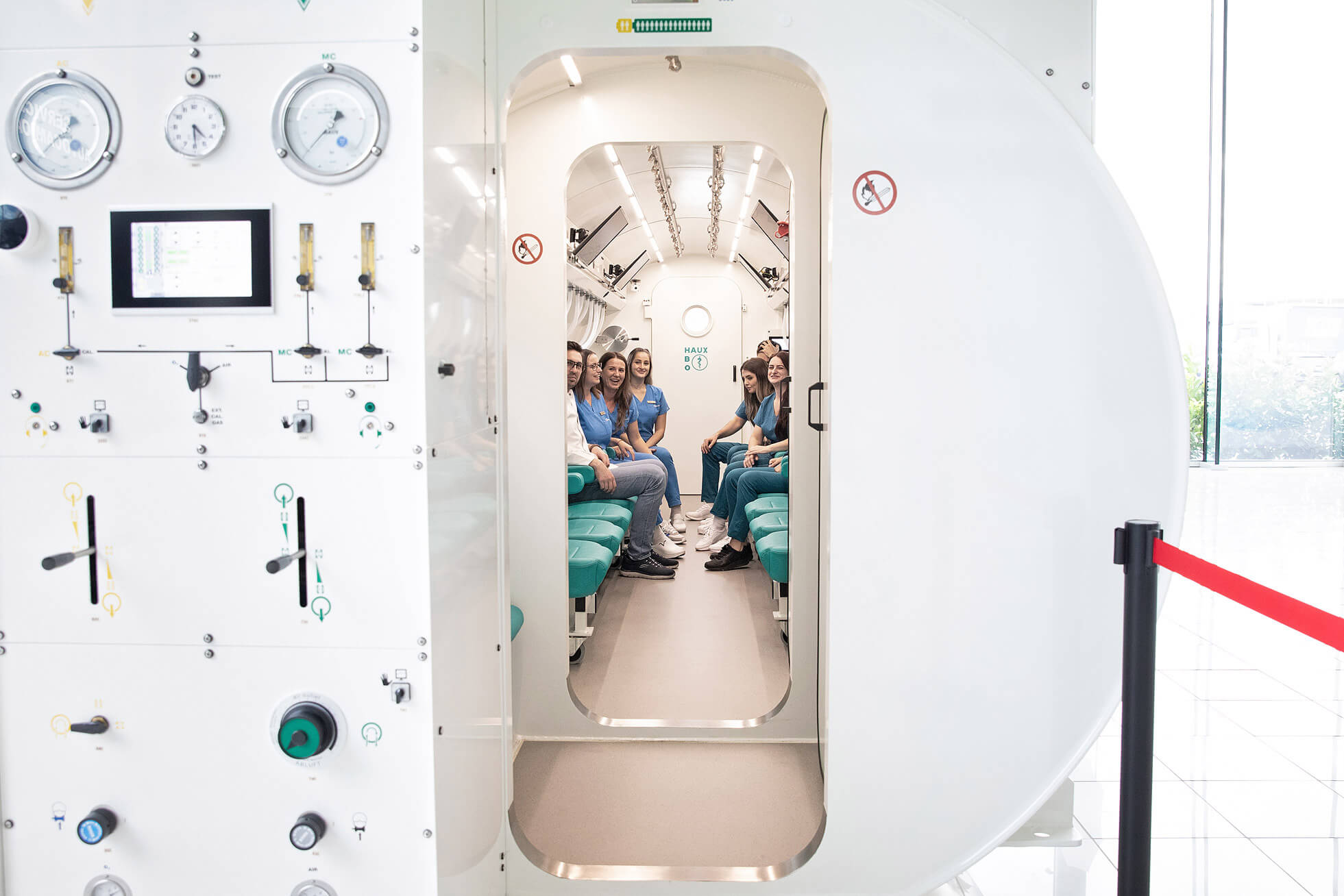
Cum stimulează terapia hiperbară producția naturală de peptide în corp
Există o cale prin care mecanismele biologice ale peptidelor regenerative pot fi accesate fără riscurile unui produs neautorizat: stimularea producției lor de către propriul organism. Terapia hiperbară medicală face exact acest lucru, având în spate decenii de dovezi clinice umane.
Când un pacient intră într-o cameră hiperbară și respiră oxigen 100% la o presiune de 2–3 ori mai mare decât cea normală, corpul nu primește o substanță chimică din exterior. Primește un semnal fizic precis, la care răspunde producând el însuși moleculele de care are nevoie pentru reparație. VEGF, factorul care comandă formarea de vase noi de sânge în zonele ischemice. BDNF, factorul care hrănește și protejează neuronii după un AVC sau o leziune neurologică. SDF-1, molecula care funcționează ca un sistem de navigație pentru celulele stem, chemându-le din măduva osoasă exact spre zona lezată. Toate acestea sunt peptide și factori de creștere endogeni, adică produși de corp, nu introduși din exterior.
Ceea ce este remarcabil din perspectiva cercetării peptidice este că acestea sunt exact moleculele pe care oamenii de știință încearcă să le reproducă sintetic în laboratoare. BPC-157 stimulează VEGF. TB-500 mobilizează celule progenitoare spre zone lezate, similar SDF-1. CJC-1295 activează o cascadă hormonală care susține reparația tisulară. Terapia hiperbară activează toate aceste procese simultan, nu prin introducerea unor molecule externe cu statut incert, ci prin crearea condițiilor în care corpul le produce singur, în dozele pe care le reglează natural și sub supraveghere medicală continuă. Nu este o alternativă de compromis față de peptidele sintetice. Este, în multe privințe, mecanismul original pe care știința peptidelor încearcă să îl imite.
De ce terapia hiperbară este alegerea sigură astăzi
Peptidele despre care am vorbit în acest articol, BPC-157, TB-500, CJC-1295, Ipamorelin, au ceva în comun: rezultatele din laborator sunt promițătoare, dar studiile pe oameni sunt încă insuficiente pentru ca vreun medic să le poată recomanda ca tratament. Nu înseamnă că știința din spate este greșită. Înseamnă pur și simplu că drumul de la testarea pe animale la tratarea în siguranță a oamenilor este lung, costisitor și, pentru multe dintre aceste molecule, încă neparcurs complet. Până la finalizarea acestui drum, ele rămân substanțe destinate cercetării, nu consumului uman.
Terapia hiperbară se află într-o poziție complet diferită. Nu este o noutate și nu este o promisiune, este o metodă medicală folosită de peste șase decenii în spitale și clinici din întreaga lume, cu sute de studii realizate pe pacienți umani reali și cu protocoale recunoscute oficial de organismele medicale europene și internaționale. Un articol de sinteză publicat în 2025 în PMC, "Application and Progress of Hyperbaric Oxygen Therapy in Cardiovascular Diseases", documentează că terapia hiperbară protejează mușchiul inimii după un infarct, stimulează formarea de vase noi de sânge în zonele afectate și îmbunătățește capacitatea vaselor de a funcționa normal. Toate acestea sunt efecte măsurate la oameni, nu doar în experimente pe animale.
În recuperarea după AVC, rezultatele sunt la fel de clare. Un studiu publicat în PLOS ONE în 2013, "Hyperbaric Oxygen Induces Late Neuroplasticity in Post Stroke Patients", a arătat ceva remarcabil: pacienți cu deficite neurologice rămase după un AVC, la doi ani de la eveniment, adică într-o perioadă în care creierul nu mai recuperează spontan, au prezentat îmbunătățiri reale după 40 de ședințe de terapie hiperbară. Mai mult, pe imagistica cerebrală s-a putut vedea că zone din creier care nu mai funcționau s-au „reactivat". Aceasta se numește neuroplasticitate, capacitatea creierului de a-și forma noi conexiuni, și este, practic, baza oricărei recuperări neurologice.
Un alt avantaj concret al terapiei hiperbare este că știi exact ce primești. Potrivit StatPearls / NIH, „Hyperbaric Cardiovascular Effects", efectele terapiei hiperbare sunt bine documentate și reproductibile: oxigenul se dizolvă în sânge în cantități de până la 20 de ori mai mari decât în mod normal, ajungând în țesuturi chiar și acolo unde circulația este slabă, cu efecte antiinflamatorii și de stimulare a regenerării bine caracterizate. Într-o clinică medicală certificată, precum Hyperbarium, fiecare ședință se desfășoară cu oxigen 100%, la o presiune standardizată, cu echipamente verificate și sub supraveghere medicală continuă. Nu există surprize legate de calitatea produsului sau de doză, probleme reale în cazul peptidelor de cercetare cumpărate online, unde nimeni nu garantează că flaconul conține exact ce scrie pe etichetă.
Viitorul peptidelor: unde se îndreaptă cercetarea
Cercetarea peptidelor terapeutice se află, în 2025–2026, într-un moment interesant. Nu mai suntem în faza în care oamenii de știință abia descoperă că aceste molecule există și că pot face lucruri remarcabile.
Câteva molecule se află deja în studii clinice de fază I și II, adică sunt testate pe oameni pentru prima oară, în grupuri mici de voluntari, pentru a evalua siguranța și dozele optime. Altele sunt în faza de optimizare a formulării: cercetătorii caută soluții pentru a le face stabile, absorbabile și administrabile convenabil, fără a le pierde activitatea biologică. Un studiu publicat în Biomolecules în 2025, "Bioactive peptides: from preclinical to clinical studies", identifică câteva direcții prioritare: peptide care ajută la controlul colesterolului, peptide cu efect antiinflamator direct pe vasele de sânge și peptide care modulează sisteme hormonale cu impact metabolic larg. Toate acestea sunt domenii în care bolile cronice de mare prevalență precum boli cardiovasculare, diabet, obezitate, au nevoie urgentă de soluții noi.
În domeniul îngrijirii pielii, progresul este deja vizibil. Noi variante ale GHK-Cu și ale peptidelor de matrice extracelulară sunt evaluate pentru formulări medicale avansate, dincolo de cosmetică, în tratamentul plăgilor cronice, al cicatricilor patologice și al afecțiunilor dermatologice inflamatorii. În oncologie, peptidele antimicrobiene și cele de semnalizare imunitară reprezintă o frontieră activă, cu câteva molecule deja în studii clinice pentru anumite tipuri de cancer. În neurologie, peptidele neurotrofice, moleculele care hrănesc și protejează neuronii, sunt studiate ca potențiale instrumente în Alzheimer, Parkinson și recuperarea post-traumatică.
Există și un obstacol structural pe care cercetarea peptidică trebuie să îl depășească: mulți dintre cei mai promitenți compuși nu pot fi brevetați, deoarece sunt derivați din secvențe biologice naturale. Fără brevet, companiile farmaceutice au stimulente financiare reduse să investească sute de milioane de euro în studii clinice complete. Acesta este, paradoxal, unul dintre motivele pentru care unele peptide cu rezultate preclinice excelente rămân ani de zile în zona cercetare, nu pentru că știința ar fi slabă, ci pentru că modelul economic al cercetării clinice nu favorizează moleculele care nu pot fi proprietatea exclusivă a unei companii.
Ceea ce este cert este că peptidele nu sunt o modă trecătoare. Ele sunt parte din biologia fundamentală a oricărui organism viu, și înțelegerea modului în care pot fi folosite terapeutic va continua să avanseze. Unele vor deveni medicamente aprobate. Altele vor rămâne în zona cosmeticelor și a suplimentelor cu dovezi solide. Și altele, cele mai complexe, vor mai aștepta câțiva ani până când studiile clinice la om vor confirma sau vor infirma promisiunile din laborator. Până atunci, cel mai bun lucru pe care îl poate face un pacient informat este să înțeleagă distincția dintre dovezi și promisiuni, și să ia orice decizie terapeutică împreună cu un medic care cunoaște atât potențialul, cât și limitele acestui domeniu fascinant.




