
A cikket áttekintette: Dr. Sturz Ciprian, Dr. Tîlvescu Cătălin és Dr. Alina Vasile
Minden, amit a peptidekről tudni érdemes: a regeneráció tudományától a kutatási protokollokig
- Mik azok a peptidek?
- Miért érdekli a peptidek a kardiovaszkuláris orvoslást
- Injektálható peptidek: a legkutatottabbak és a legtöbbet vitatottak
- Orális peptidek: biológiai kihívás és valódi ígéret
- Topikális peptidek: a legelérhetőbbek és a legerősebb humán bizonyítékokkal
- Matrixyl (Palmitoil Pentapeptida-4), a referencia anti-aging peptid
- Argireline (Acetil Hexapeptida-3) — a botox kozmetikai alternatívája
- Orális hidrolizált kollagén peptidek — mit ad a belső pótlás
- GHK-Cu — a réztartalmú peptid három évtizednyi kutatással
- Topikális Thymosin Beta-4 — a nehezen gyógyuló sebek specialistája
- Kutatási peptidek: ígéretesek laboratóriumban, egyelőre nem engedélyezettek humán használatra
- Hogyan serkenti a hiperbárikus terápia a peptidek természetes termelését a szervezetben
- Miért a hiperbárikus terápia a biztonságos választás ma
- A peptidek jövője: merre halad a kutatás
Ha mostanában hallott a peptidekről, akár egy rendelőben, az interneten vagy egy hosszú élettartamról szóló podcastben, és azon gondolkodott, mik ezek, valóban működnek-e, és biztonságosak-e, akkor jó helyen jár. A peptidek a modern orvoslás egyik leggyakrabban tárgyalt témájává váltak, nem véletlenül. A kutatók felfedezik, hogy ezek az apró molekulák, amelyeket a szervezetünk természetesen termel, figyelemre méltó regeneratív potenciállal rendelkeznek, a szövetgyógyulástól és a szív egészségétől kezdve egészen a stroke utáni felépülésig.
De minden lelkesedés előtt fontos pontosan megérteni, mit tudunk, mit nem tudunk még, és hol húzódik a határ az ígéret és a klinikai valóság között. Ez a cikk mindent elmagyaráz: a peptidek típusait, mit mondanak az orvosi tanulmányok, hogyan használják őket, és végül azt is, miért marad jelenleg a hiperbárikus orvosi terápia az egyik legbiztonságosabb és legjobban dokumentált lehetőség a szív és az agy egészségének támogatására.
Mik azok a peptidek?
Képzeld el a testedben lévő fehérjéket hosszú láncokként. Minden láncszem egy aminosav. A peptid gyakorlatilag egy rövid szakasz egy ilyen láncból, vagyis néhány egymáshoz kapcsolódó láncszem, általában 2 és 50 aminosav között. Amikor a lánc hosszabb lesz 50-nél, már fehérjéről beszélünk.
A peptidek különlegessége nem a kis méretük, hanem az a pontosság, amellyel működnek. Minden peptid úgy illeszkedik, mint egy kulcs egy adott zárba, a sejtek felszínén található receptorba, és egy pontos üzenetet közvetít: „termelj kollagént", „hozz létre új ereket", „csökkentsd a gyulladást", „javítsd a sérült szövetet". Az emberi test természetesen több száz ilyen hírvivőt termel. Az inzulin egy peptid. Az oxitocin egy peptid. A növekedési hormon peptideken keresztül hat. A peptidterápia alapgondolata egyszerű: ha ezek a molekulák már léteznek a szervezetben és hasznos dolgokat végeznek, vajon felhasználhatjuk vagy serkenthetjük őket terápiás céllal?
A kutatás válasza: igen, de sok árnyalattal.
Miért érdekli a peptidek a kardiovaszkuláris orvoslást
A kardiovaszkuláris rendszer valószínűleg az a terület, ahol a peptidek a legnagyobb regenerációs potenciált mutatták. Az ok egyszerű: a szív egy olyan szerv, amelynek rendkívül korlátozott az önregeneráló képessége. Míg a vese vagy a máj bizonyos mértékig képes kompenzálni, a szív nem tudja hatékonyan pótolni az infarktus után elvesztett izomsejteket. Itt lépnek be a peptidek mint egy olyan regenerációs folyamat lehetséges „építészei", amelyet a szervezet önmagában nem tud befejezni.
Az epidemiológiai helyzet pedig sürgetővé teszi ezt a kérdést. A Országos Közegészségügyi Intézet szerint a szív- és érrendszeri betegségek a Romániában regisztrált halálesetek közel 56%-áért felelősek. A Egészségügyi Minisztérium adatai szerint Romániában a kardiovaszkuláris halálozási arány 2,5-szer magasabb az EU átlagánál.
A magas vérnyomás pedig, mint az egyik fő kockázati tényező, a romániai felnőttek több mint 45%-át érinti, a Román Hipertónia Társaság szerint. Ezek a számok nem elvont statisztikák. Egy olyan közegészségügyi válságot írnak le, amelyben minden új terápiás lehetőséget komolyan kell venni.
Injektálható peptidek: a legkutatottabbak és a legtöbbet vitatottak
Az injektálható peptidek jelentik azt a kategóriát, amely mögött a legnagyobb kutatási volumen áll, és egyben a legnagyobb érdeklődést is kiváltják a tájékozott közönség körében. Az ok, amiért az injekciót részesítik előnyben a tablettával szemben, egyszerű: a gyomrunk ugyanúgy lebontja a peptideket, mint bármely más fehérjét. Az emésztőenzimek darabokra bontják őket, mielőtt az aktív molekula eljutna a véráramba. A szubkután (bőr alá) vagy intramuszkuláris beadás megkerüli ezt a problémát, és lehetővé teszi, hogy a peptid érintetlenül jusson a keringésbe.
BPC-157 — a gyomornedvből származó peptid
A bőrre történő közvetlen alkalmazás a peptidek beadásának legegyszerűbb módja, és meglepő módon ez az a terület, ahol a legtöbb, már validált klinikai alkalmazás található. A kozmetikai peptidek kevesebb mint két évtized alatt a biokémiai laboratóriumok szűk világából emberek millióinak mindennapi bőrápolási rutinjába kerültek.
Miért működik a topikális alkalmazás a peptidek esetében, miközben láttuk, hogy az orális út komoly korlátokkal jár? A kis molekulájú peptidek képesek áthatolni a szarurétegen, vagyis a bőr felszíni rétegén, és eljutni a dermiszbe, abba a mélyebb rétegbe, ahol a fibroblasztok találhatók. A fibroblasztok a bőr „üzemsejtjei”: kollagént, elasztint és hialuronsavat termelnek, vagyis pontosan azokat a molekulákat, amelyek a feszességért, rugalmasságért és hidratáltságért felelősek. Ott a bőrre való peptidek pontos biológiai üzeneteket közvetítenek: „termelj több kollagént”, „hozz létre új ereket”, „javítsd helyre a bőrgátat”, „csillapítsd a gyulladást”. Az öregedő vagy károsodott bőr nem kap elegendő mennyiségben ilyen utasításokat, a topikális peptidek pedig kívülről juttatják vissza ezeket.
Matrixyl (Palmitoil Pentapeptida-4), a referencia anti-aging peptid
A Matrixyl valószínűleg a világ leginkább kutatott anti-aging kozmetikai peptidje. Kereskedelmi elnevezését a palmitoil pentapeptida-4-re használják, amely egy szintetikus molekula, és amelyet úgy terveztek, hogy utánozza a lebomlott kollagén fragmentumait. Így a bőrt „becsapja”, mintha sérült kollagén lenne jelen, és ezzel arra ösztönzi, hogy kompenzációként új kollagént termeljen.
A Matrixyllel kapcsolatos klinikai vizsgálatok következetesek: egy palmitoil pentapeptida-4 alapú formuláció napi használat mellett 8–12 hét után akár 45%-kal is csökkentette a ráncok mélységét a placebocsoporthoz képest, a Peptide Journal által összesített adatok szerint. A L'Oréal Paris, a világ egyik legnagyobb kozmetikai gyártója, egy olyan tanulmányra hivatkozik, amely szerint a peptidek topikális alkalmazás esetén akár 30%-kal is fokozhatják a bőr kollagéntermelését, látható hatással a ráncok csökkentésére és a feszesség javítására. A Matrixyl 3000, egy továbbfejlesztett változat, amely a palmitoil tetrapeptida-7-et palmitoil oligopeptidával kombinálja, hasonló vagy még jobb eredményeket mutatott, további előnyökkel a bőr öregedésével összefüggő alacsony fokú krónikus gyulladás csökkentésében.
A mechanizmus szempontjából: a Matrixyl nem közvetlenül a ráncokra hat, hanem azt a struktúrát építi újjá, amelynek a ráncok csupán tünetei. Ez alapvetően eltér a klasszikus hidratálóktól, amelyek ideiglenesen „feltöltik” a bőrt, vagy a töltőeljárásoktól, amelyek kívülről adnak hozzá térfogatot. A Matrixyl arra ösztönzi a bőrt, hogy a saját tartószerkezeteit állítsa helyre.
Argireline (Acetil Hexapeptida-3) — a botox kozmetikai alternatívája
Az Argireline-t gyakran „krémes botoxnak” nevezik, ami leegyszerűsítő összehasonlítás, de nem teljesen téves. A mechanizmus hasonló: a botox blokkolja az acetilkolin felszabadulását (azt a kémiai anyagot, amelyen keresztül az idegek utasítják az izmokat az összehúzódásra), így átmenetileg megbénítja azokat az arcizmokat, amelyek a mimikai ráncokat okozzák. Az Argireline hasonló, de enyhébb mechanizmussal hat: beavatkozik a SNARE-komplex működésébe, vagyis abba a molekuláris mechanizmusba, amelyen keresztül a neuronok neurotranszmittereket szabadítanak fel, részben csökkentve az arcizmok összehúzódásának intenzitását, a botulinumtoxin bénító hatása nélkül.
Egy randomizált, placebo-kontrollált vizsgálat, amelyet az International Journal of Cosmetic Science közölt, "A synthetic hexapeptide (Argireline) with antiwrinkle activity", kimutatta, hogy az Argireline egy nem toxikus peptid, amelynek ránctalanító aktivitása mechanikailag a botulinumtoxinéhoz hasonlítható, de neurotoxicitás nélkül. Egy második klinikai vizsgálat, amely a Skin Research and Technology folyóiratban jelent meg, "The anti-wrinkle efficacy of argireline", 60 alanyt vizsgált, akik naponta kétszer, négy héten át alkalmazták az Argireline-t a szemkörnyéki ráncokra. Eredmény: a kezelt csoport 48,9%-ánál jelentkezett ráncjavulás, szemben a placebocsoport 0%-ával, az objektíven mért bőrérdességi paraméterek jelentős csökkenésével.
A botulinumtoxinnal szembeni előnye nyilvánvaló: az Argireline otthon alkalmazható, injekciók nélkül, aszimmetrikus bénulás kockázata nélkül, és az ismételt orvosi kezelések költségei nélkül. A hátránya ugyanilyen valós: a hatások mérsékeltebbek, és a használat abbahagyásával megszűnnek, az Argireline nem építi újjá a bőr szerkezetét, hanem átmenetileg csökkenti azokat az izomösszehúzódásokat, amelyek mélyítik a mimikai ráncokat. Ennek a peptidnek a legjobb jelöltjei azok az emberek, akiknek mimikai ráncaik vannak (homlok, szemzugok, száj környéki terület), nem pedig azok, akiknek a ráncai kollagénvesztés vagy hosszan tartó napfény-expozíció miatt alakultak ki.
Orális hidrolizált kollagén peptidek — mit ad a belső pótlás
A közvetlen topikális alkalmazáson túl az orálisan bevitt kollagén peptidek az elmúlt években rendkívüli népszerűségre tettek szert, és más orális peptidekhez képest kivételes módon léteznek olyan humán klinikai vizsgálatok, amelyek részben alátámasztják ezt a népszerűséget. A hidrolizált kollagén (vagyis a kis, felszívódó peptidekre bontott kollagén) több randomizált kontrollált vizsgálatban is mérhető előnyöket mutatott a bőr számára.
Egy 105, 24 és 50 év közötti nő bevonásával végzett klinikai vizsgálat, akik hat hónapon át kollagén peptideket fogyasztottak, simább, rugalmasabb és láthatóan javult megjelenésű bőrt dokumentált minden résztvevőnél. A PEPTAN hidrolizált kollagénnel végzett vizsgálatok azt mutatták, hogy 12 hét pótlás után a dermisz kollagénsűrűsége 8,83%-kal nőtt a placebocsoporthoz képest, ahol nem észleltek változást. Miért működik az orális kollagén, ha korábban azt mondtuk, hogy a peptidek lebomlanak a gyomorban? Pontosan azért, mert a hidrolizált kollagén peptidek már előemésztett, kis fragmentumokból, dipeptidekből és tripeptidekből állnak, amelyek viszonylag épen felszívódhatnak a bél nyálkahártyáján keresztül, bekerülnek a keringésbe, és ott serkentik a dermisz fibroblasztjait saját kollagén termelésére.
GHK-Cu — a réztartalmú peptid három évtizednyi kutatással
A GHK-Cu (glicil-L-hisztidil-L-lizin-réz) a biokémia történetének egyik legkutatottabb topikális peptidje. Ez egy tripeptid, vagyis mindössze három aminosavból álló peptid, amely természetes módon jelen van a fiatal emberek vérplazmájában. 20 éves korban a vérszintje körülbelül 200 ng/mL; 60 éves korban 80 ng/mL-re csökken. A kutatók megfigyelték, hogy ez a csökkenés egybeesik a szöveti regenerációs képesség életkorral járó hanyatlásával.
Egy 2018-ban az International Journal of Molecular Sciences folyóiratban megjelent tanulmány, "Regenerative and Protective Actions of the GHK-Cu Peptide", dokumentálta, hogy a GHK-Cu serkenti az erek és az idegek növekedését, fokozza a kollagén- és elasztintermelést, csökkenti a gyulladást, és aktiválja a szövet antioxidáns rendszerét. Továbbá egy 71 nő bevonásával végzett kontrollált klinikai vizsgálat azt mutatta, hogy a 12 héten át alkalmazott GHK-Cu tartalmú arckrém növelte a dermisz sűrűségét és vastagságát, csökkentette a ráncokat és javította a bőr textúráját, a kollagéntermelés fokozásában jobb eredményeket mutatva, mint a C-vitamin vagy a retinsav.
Topikális Thymosin Beta-4 — a nehezen gyógyuló sebek specialistája
A Thymosin Beta-4, amikor közvetlenül egy sebre vagy bőrelváltozásra topikálisan alkalmazzák, figyelemre méltó hatásokat mutatott kutatási modellekben. Egy 2024-ben a Journal of Tissue Engineering folyóiratban megjelent tanulmány, "Discovery of Bioactive Peptides as Therapeutic Agents for Skin Wound Repair", dokumentálja, hogy a TB-4 fokozta a re-epitelizációt (vagyis a seb új bőrrel való fedését) és a helyi angiogenezist, különösen erős aktivitással a helyreállító sejtek sérült terület felé történő vándorlásának serkentésében. Ez értékes tulajdonság krónikus sebek, például diabéteszes fekélyek, felfekvések vagy besugárzás utáni sebek esetén, amelyek jelentős klinikai problémát jelentenek, és ahol a jelenlegi terápiás lehetőségek korlátozottak.
Kutatási peptidek: ígéretesek laboratóriumban, egyelőre nem engedélyezettek humán használatra
Itt az ideje tisztázni egy olyan kérdést, amelyet az internet gyakran kétértelműen kezel: a fent tárgyalt peptidek közül soknak a jogi és orvosi státuszát.
Az Európai Unióban egy anyag csak akkor adható gyógyszerként embereknek, ha engedélyt kapott az EMA-tól (Európai Gyógyszerügynökség), miután végigment az I., II. és III. fázisú klinikai vizsgálatokon, amelyek mind a biztonságosságot, mind a hatékonyságot bizonyítják. Az olyan peptidek, mint a BPC-157, TB-500, CJC-1295 vagy az Ipamorelin nem rendelkeznek ilyen engedéllyel. Jogilag „kutatási anyagként” gyárthatók és értékesíthetők, ami azt jelenti, hogy kizárólag laboratóriumi használatra, nem pedig emberi fogyasztásra szánják őket.
Egy 2026-ban megjelent cikk az európai peptidpiac fejlődéséről azt mutatja, hogy az európai hatóságok fokozottan ellenőrzik azokat a cégeket, amelyek ezeket az anyagokat „research only” (csak kutatási célra) címkével látják el, de nyilvánvalóan emberi fogyasztásra népszerűsítik őket. Ez valós probléma: a szabályozás hiánya azt jelenti, hogy a tisztaságot, a pontos koncentrációt és a szennyeződések hiányát semmilyen tanúsító szerv nem garantálja.
A helyes hozzáállás ezekhez a molekulákhoz sem a teljes elutasítás, sem a kritikátlan lelkesedés. Kutatásuk ígéretes, és érdemes folytatni. De jelenleg az emberi alkalmazásuk kontrollált kutatási protokollon kívül ismeretlen kockázatokkal jár. Egy felelős orvos nem ajánlhatja használatukat a standard klinikai gyakorlatban, éppen a teljes humán klinikai bizonyítékok hiánya miatt.
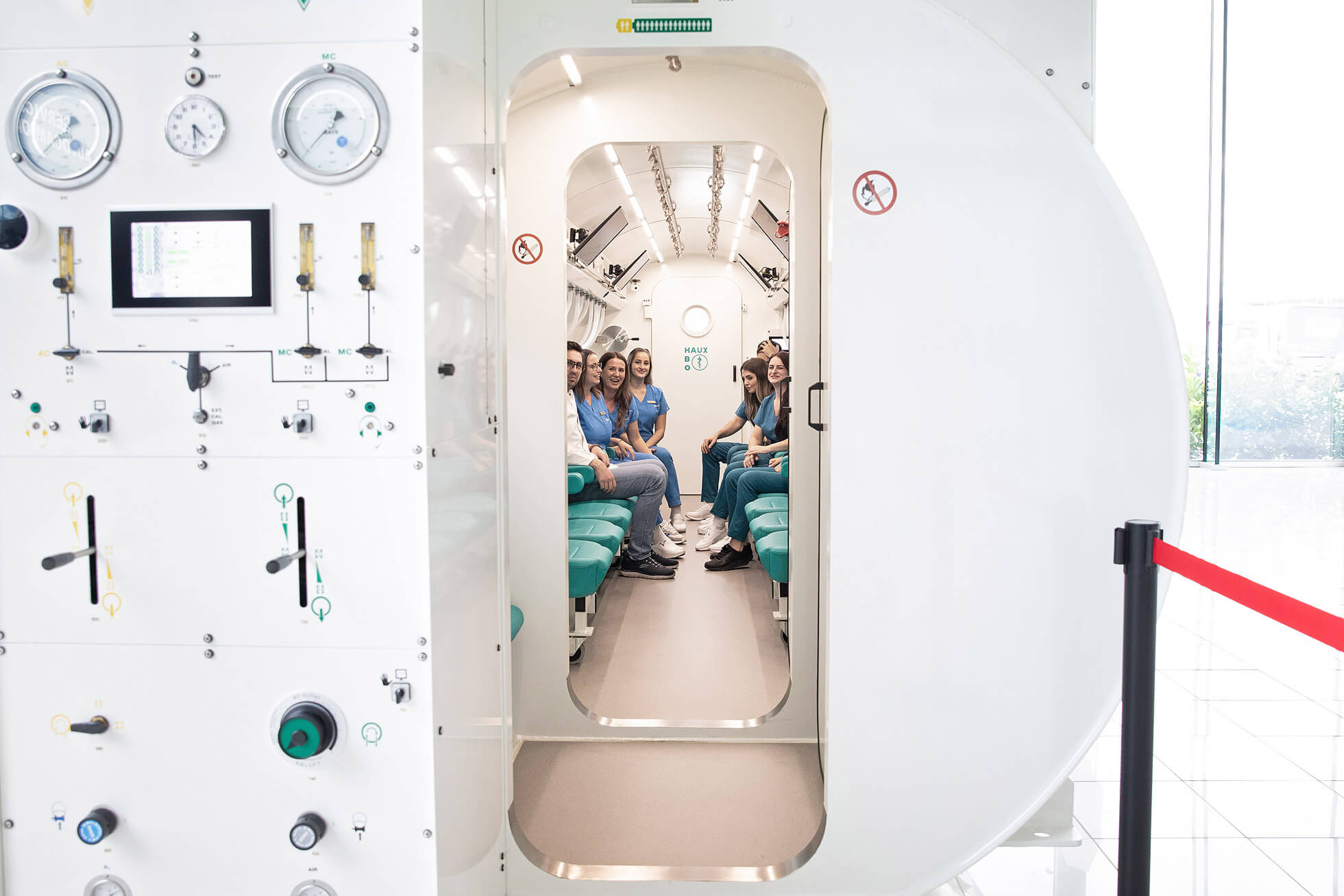
Hogyan serkenti a hiperbárikus terápia a peptidek természetes termelését a szervezetben
Létezik egy út, amelyen keresztül a regeneratív peptidek biológiai mechanizmusai egy nem engedélyezett termék kockázatai nélkül is elérhetők: saját szervezetünk általi termelésük serkentése. A hiperbárikus orvosi terápia pontosan ezt teszi, mögötte évtizedekre visszanyúló humán klinikai bizonyítékokkal.
Amikor egy beteg belép egy hiperbárikus kamrába, és 100%-os oxigént lélegez be a normálisnál 2–3-szor nagyobb nyomáson, a test nem kívülről kap egy kémiai anyagot. Egy pontos fizikai jelet kap, amelyre úgy reagál, hogy maga termeli meg azokat a molekulákat, amelyekre a helyreállításhoz szüksége van. VEGF, az a faktor, amely az új erek kialakulását irányítja az iszkémiás területeken. BDNF, az a faktor, amely táplálja és védi a neuronokat stroke vagy neurológiai sérülés után. SDF-1, az a molekula, amely a őssejtek navigációs rendszereként működik, és a csontvelőből pontosan a sérült területre hívja őket. Mindezek endogén peptidek és növekedési faktorok, vagyis a szervezet által termelt, nem pedig kívülről bevitt anyagok.
Ami figyelemre méltó a peptidkutatás szempontjából, hogy pontosan ezek azok a molekulák, amelyeket a tudósok laboratóriumokban szintetikusan próbálnak reprodukálni. A BPC-157 serkenti a VEGF-et. A TB-500 a sérült területek felé mobilizálja a progenitor sejteket, az SDF-1-hez hasonlóan. A CJC-1295 egy hormonális kaszkádot aktivál, amely támogatja a szöveti helyreállítást. A hiperbárikus terápia mindezeket a folyamatokat egyszerre aktiválja, nem bizonytalan státuszú külső molekulák bevitelével, hanem olyan feltételek megteremtésével, amelyek között a szervezet maga termeli meg ezeket, természetesen szabályozott dózisokban és folyamatos orvosi felügyelet mellett. Ez nem kompromisszumos alternatívája a szintetikus peptideknek. Sok tekintetben ez az az eredeti mechanizmus, amelyet a peptidtudomány utánozni próbál.
Miért a hiperbárikus terápia a biztonságos választás ma
Azoknak a peptideknek, amelyekről ebben a cikkben szó volt — BPC-157, TB-500, CJC-1295, Ipamorelin — van valami közös jellemzőjük: a laboratóriumi eredmények ígéretesek, de az embereken végzett vizsgálatok még nem elegendőek ahhoz, hogy bármely orvos kezelésként ajánlani tudja őket. Ez nem azt jelenti, hogy a mögöttük álló tudomány téves. Egyszerűen azt jelenti, hogy az állatkísérletektől az emberek biztonságos kezeléséig vezető út hosszú, költséges, és sok ilyen molekula esetében még nem teljesen bejárt. Amíg ez az út be nem fejeződik, ezek továbbra is kutatásra szánt anyagok maradnak, nem emberi fogyasztásra.
A hiperbárikus terápia teljesen más helyzetben van. Nem újdonság, és nem ígéret, hanem egy több mint hat évtizede használt orvosi módszer a világ kórházaiban és klinikáin, több száz valódi humán beteggel végzett vizsgálattal és az európai, illetve nemzetközi orvosi szervezetek által hivatalosan elismert protokollokkal. Egy 2025-ben a PMC-ben megjelent összefoglaló cikk, "Application and Progress of Hyperbaric Oxygen Therapy in Cardiovascular Diseases", dokumentálja, hogy a hiperbárikus terápia megvédi a szívizmot infarktus után, serkenti az új erek kialakulását az érintett területeken, és javítja az erek normális működési képességét. Mindezek embereken mért hatások, nem csupán állatkísérletek eredményei.
A stroke utáni rehabilitációban az eredmények ugyanolyan egyértelműek. Egy 2013-ban a PLOS ONE folyóiratban megjelent tanulmány, "Hyperbaric Oxygen Induces Late Neuroplasticity in Post Stroke Patients", valami figyelemre méltót mutatott: azoknál a betegeknél, akiknél a stroke után két évvel is megmaradtak neurológiai hiánytünetek — tehát abban az időszakban, amikor az agy már nem regenerálódik spontán —, 40 hiperbárikus kezelést követően valódi javulás jelentkezett. Sőt, az agyi képalkotó vizsgálatokon látható volt, hogy olyan agyterületek, amelyek már nem működtek, „újraaktiválódtak”. Ezt neuroplaszticitásnak nevezik, vagyis az agy új kapcsolatok kialakítására való képességének, és ez gyakorlatilag minden neurológiai rehabilitáció alapja.
A hiperbárikus terápia egy másik kézzelfogható előnye, hogy pontosan tudja, mit kap. A StatPearls / NIH szerint a „Hyperbaric Cardiovascular Effects” jól dokumentáltak és reprodukálhatók: az oxigén a normálisnál akár 20-szor nagyobb mennyiségben oldódik a vérben, és olyan szövetekhez is eljut, ahol a keringés gyenge, jól jellemzett gyulladáscsökkentő és regenerációt serkentő hatásokkal. Egy tanúsított orvosi klinikán, mint például a Hyperbarium, minden kezelés 100%-os oxigénnel, standardizált nyomáson, ellenőrzött berendezésekkel és folyamatos orvosi felügyelet mellett zajlik. Nincsenek meglepetések a termék minőségével vagy dózisával kapcsolatban, amelyek valós problémák az interneten vásárolt kutatási peptidek esetében, ahol senki sem garantálja, hogy az ampulla pontosan azt tartalmazza, ami a címkén szerepel.
A peptidek jövője: merre halad a kutatás
A terápiás peptidek kutatása 2025–2026-ban izgalmas pillanatban van. Már nem ott tartunk, hogy a tudósok csak most fedezik fel, hogy ezek a molekulák léteznek, és figyelemre méltó dolgokra képesek.
Néhány molekula már az I. és II. fázisú klinikai vizsgálatokban van, vagyis először tesztelik embereken, kis önkéntes csoportokban, hogy felmérjék a biztonságosságot és az optimális dózisokat. Mások a formuláció optimalizálásának szakaszában vannak: a kutatók olyan megoldásokat keresnek, amelyekkel stabillá, felszívódóvá és kényelmesen adagolhatóvá tehetők anélkül, hogy elveszítenék biológiai aktivitásukat. Egy 2025-ben a Biomolecules folyóiratban megjelent tanulmány, "Bioactive peptides: from preclinical to clinical studies", több prioritást élvező irányt azonosít: peptideket, amelyek segítenek a koleszterin szabályozásában, peptideket, amelyek közvetlen gyulladáscsökkentő hatással vannak az erekre, és peptideket, amelyek széles anyagcsere-hatású hormonális rendszereket modulálnak. Mindezek olyan területek, ahol a nagy prevalenciájú krónikus betegségek, mint a szív- és érrendszeri betegségek, a diabétesz és az elhízás sürgősen új megoldásokat igényelnek.
A bőrápolás területén a fejlődés már látható. A GHK-Cu és az extracelluláris mátrix peptidek új változatait fejlett orvosi formulációkhoz értékelik, a kozmetikán túl, krónikus sebek, kóros hegek és gyulladásos bőrbetegségek kezelésére. Az onkológiában az antimikrobiális peptidek és az immunjelátviteli peptidek aktív határterületet jelentenek, néhány molekula már klinikai vizsgálatokban szerepel bizonyos daganattípusok esetén. A neurológiában a neurotróf peptideket — az idegsejteket tápláló és védő molekulákat — potenciális eszközként vizsgálják Alzheimer-kór, Parkinson-kór és traumát követő rehabilitáció esetén.
Van egy strukturális akadály is, amelyet a peptidkutatásnak le kell küzdenie: a legígéretesebb vegyületek közül sok nem szabadalmaztatható, mert természetes biológiai szekvenciákból származik. Szabadalom nélkül a gyógyszergyáraknak kisebb pénzügyi ösztönzésük van arra, hogy több százmillió eurót fektessenek teljes klinikai vizsgálatokba. Paradox módon ez az egyik oka annak, hogy néhány kiváló preklinikai eredménnyel rendelkező peptid évekig a kutatási zónában marad, nem azért, mert a tudomány gyenge lenne, hanem mert a klinikai kutatás gazdasági modellje nem kedvez azoknak a molekuláknak, amelyek nem válhatnak egyetlen cég kizárólagos tulajdonává.
Ami biztos, hogy a peptidek nem múló divathullámot jelentenek. Minden élő szervezet alapvető biológiájának részei, és annak megértése, hogyan használhatók terápiásan, tovább fog fejlődni. Néhányukból engedélyezett gyógyszer lesz. Mások a kozmetikumok és a szilárd bizonyítékokkal rendelkező étrend-kiegészítők világában maradnak. Megint mások, a legösszetettebbek, még néhány évig várni fognak, amíg a humán klinikai vizsgálatok megerősítik vagy cáfolják a laboratóriumi ígéreteket. Addig a legjobb, amit egy tájékozott beteg tehet, hogy megérti a bizonyítékok és az ígéretek közötti különbséget, és minden terápiás döntést olyan orvossal együtt hoz meg, aki ismeri ennek a lenyűgöző területnek a lehetőségeit és korlátait is.




